en
names in breadcrumbs


El gripau raucador de ventre groc és una espècie d'amfibi que viu a Europa.[1]
Mesura uns 5 cm de llarg i té tota la part inferior del seu cos de color groc o groc ataronjat amb petites taques negres, inclús la part inferior de les seves potes i dits. La seva part superior no destaca en especial, sent de color marró verdós.
Aquesta espècie es pot trobar en gran varietat d'hàbitats, en boscos de coníferes i boscos caducifolis, des de pèlags als pobles, rius, llacunes, pantans, llacs i gairebé en qualsevol lloc on hi hagi aigua estancada, inclús en l'aigua en neumàtics abandonats.
Es distribueix per una gran part de l'Europa central i el sud. Va des del centre de França, Suïssa, Alemanya, nord-est d'Itàlia la zona dels Balcans i fins als Carpats. Es troba entre els 100 i els 2.100 metres d'altitud.[2]
Les femelles ponen fins a 100 ous que es desclouen al cap de 12 dies. Els capgrossos mesuren un 6 mm de longitud.
En general, l'espècie no es troba amenaçada. Els únics perills per l'espècie són la pèrdua d'hàbitat per culpa de la urbanització humana, la seva captura furtiva com a mascota i la seva captura com a esquer de pesca en certes regions.
Kuňka žlutobřichá (Bombina variegata Linné, 1758) je obojživelník z čeledi kuňkovití. V Česku se jedná o ohrožený druh žab.
Dosahuje velikosti 5 cm. Svrchu má hnědavou až šedozelenou barvu. Kůže je typicky bradavičnatá, přičemž bradavičky jsou hrubé na pohled i na dotek. Na hřbetě těla jsou kožní bradavičky zakončeny výrazným černým trnem na vrcholu. Hlavu má plochou, širokou a okrouhlou. Není viditelný ušní bubínek. Oční zornice jsou většinou srdcovitého či trojúhelníkovitého tvaru.
Zbarvení svrchní strany těla se liší podle místa výskytu; nejčastěji je šedé, olivově zelené nebo hnědé, může být i více do zelena. Celkově bývá kuňka žlutobřichá spíše světlejší než kuňka ohnivá. Břicho je strakaté, žluté a černé (někdy žluté a šedé nebo tmavošedé). Základní a převažující je žlutá barva (často výrazně více než 50% pokrytí břicha). Tmavé skvrny na břiše jsou posety drobnými bílými tečkami, ovšem jen řídce (na rozdíl od kuňky ohnivé).[2]
Samec kuňky žlutobřiché je menší než samice, má však silnější končetiny. V období páření se samcům objevují mozoly na vnitřní straně předloktí a na třech vnitřních prstech. Samci kuňky mají na rozdíl od samic tzv. rezonátor, který používají v době páření.[2]
Hlas tohoto obojživelníka zní velmi příjemně. Jedná se o poměrně tiché „ung“ nebo „uh“. Můžeme pozorovat zajímavě vypadající srdcovitou zornici oka.[3]
Typickém místem výskytu a rozmnožování jsou malé dočasné vodní plochy. Může se jednat i o vyjeté koleje na nezpevněných lesních cestách. Ve větší oblibě má raději vyšší polohy – od 250 do více než 1 200 m n. m. Pro kladení svých vajíček upřednostňuje prosluněná nezastíněná místa. Tato žabka je aktivní ve dne i v noci. Pokud ji zpozorujeme ve dne, často leží ve vodě nebo odpočívají na mělčině u břehu. Plave krátkými tempy. Velmi často se potápí. Pokud je vyrušena, ukryje se v bahně. Právě zde ji poslouží její svrchní zbarvení jako maskování. V případě nebezpečí na souši zaujme výstražný postoj (zvedne přední a zadní nohy, prohne hřbet) a odhalí odstrašující zbarvení břicha. Jedná se o varovný signál, který upozorňuje, že je tento živočich nejedlý. Vylučovaný kožní sekret je žíravý a může způsobit alergickou reakci. Dráždí ústní sliznici a působí odporně.
Zimu přečkává v bahně ve vodě nebo na souši zahrabaná v zemi.[4]
Jedná se výhradně o evropský druh. Vyskytuje se na západ od Francie až po karpatský masiv a od středního Německa a jižního Polska, dále Itálie a Balkán. Žije tedy také v České republice.
Její populace je široce roztroušená v sekundárních biotopech – např. kamenolomy, pískovny, štěrkovny a těžiště jílu, které jsou zaplavené mělkou, příliš nezarostlou vodou. Na Moravě jsou její populace výrazně rozšířenější a méně ohrožené než česká populace. Kuňka žlutobřichá byla také zaznamenána v Blovicích u Plzně, kde kvůli její přítomnosti bylo zastaveno bourání staré cihelny a v současné době se zde nesmí cokoliv stavět ani upravovat terén.
Během posledních třiceti let došlo ve Středních Čechách k úbytku o 90 %. Tato kuňka dokáže snést i silné organické znečištění vody. Hlavní příčinou mizení celých populací je devastace prostředí – velkoplošná aplikace biocidů, mizení a intoxikace vhodných stanovišť. V lesích je na vině používání těžké mechanizace a úpravy cest štěrkováním a asfaltováním. Dalším faktorem je zřizování skládek v místě bývalých lomů.
V České republice se jedná o silně ohrožený druh dle vyhlášky č. 395/1992 Sb.
Na jaře samci vydávají charakteristické volání. Přitom si udržují přibližně 50cm odstup. V případě přiblížení jiného samečka se jej „majitel území“ pokouší odstrčit zadníma nohama. Podle sborového volání samečků samičky snadno najdou místo rozmnožování. Samičku připravenou k rozmnožování sameček pomocí hrbolků na prstech a předloktích pevně obejme v oblasti beder (tzv. amplexus inguinalis). Sameček poté oplodní asi 150 vajíček, které samička klade jednotlivě či v malých shlucích na vodní rostlinstvo, kousky větví nebo kameny. Samice se mohou během léta rozmnožovat i několikrát. Naděje vajíček a pulců na přežití v malých nestálých vodních nádržích se tak velmi zvyšuje. Pulci se líhnou přibližně po dvou týdnech. Po dvou měsících se promění v malé žabky. Ve druhém až třetím roce života dochází k pohlavní dospělosti.
Může docházet ke křížení s kuňkou obecnou.[5]
Živí se červy, larvami komárů a jinými drobnými živočichy.
Kuňka žlutobřichá (Bombina variegata Linné, 1758) je obojživelník z čeledi kuňkovití. V Česku se jedná o ohrožený druh žab.
Die Gelbbauchunke (Bombina variegata), auch Bergunke genannt, gehört innerhalb der Klasse der Amphibien zur „urtümlichen“ Familie Bombinatoridae (in vielen Übersichten wird sie aber noch zu den Scheibenzünglern gestellt) und zur Gattung der Unken. Der kleine, spitzwarzige Froschlurch hat eine unscheinbar gefärbte Oberseite, während die Bauchseite eine leuchtend gelbe Warnfärbung aufweist. Die Art kommt regional auch in Mitteleuropa vor und bevorzugt als Lebensraum lehmige Pfützen und Kleintümpel.
Die Gelbbauchunke wurde von der Deutschen Gesellschaft für Herpetologie und Terrarienkunde zum Lurch des Jahres 2014 gekürt.[1]
Die Größe der Männchen und Weibchen liegt zwischen 35 und 56 Millimetern; in Mitteleuropa sind Kopf-Rumpf-Längen von mehr als 45 mm aber selten zu beobachten. Die Oberseite ist lehm- bis graubraun, wobei manchmal in der Nackengegend schmale dunklere Drüsenkomplexe und verwaschen helle Flecken sichtbar sind. Die Unterseite inklusive der Innenseiten der Gliedmaßen und der Finger und Zehen ist intensiv hellgelb bis orange gefärbt und mit bleigrauen bis schwarzen Flecken oder Flächen durchsetzt. Meist liegt der Gelbanteil bei mehr als der Hälfte der Fläche (gelegentlich treten auch Tiere mit fast gänzlich gelber Bauchseite auf; aber auch komplett schwarze wurden beobachtet). Weil das Zeichnungsmuster der Unterseite bei jedem Tier verschieden ist, ermöglicht dies eine individuelle Unterscheidung – etwa im Rahmen zoologischer Untersuchungen. In diesem Zusammenhang hat sich die fotografische Dokumentation der gelb-schwarzen Unterseite als zuverlässige, individuelle Identifikationsmethode bewährt. Die fotografische Erfassung (Photographic-Mark-Recapture – PMR) ist für die Tiere schonend und damit ethisch vertretbar[2][3]. Für ein erfolgreiches Monitoring ist es notwendig, die zu beobachtenden Populationen zwei- bis dreimal jährlich aufzusuchen. Geplant sind PMR-Studien, die anhand des Feuersalamanders und der Gelbbauchunke an der Universität Bielefeld und der TiHo Hannover mit Unterstützung durch den NABU Niedersachsen durchgeführt werden sollen.[4]
Gelbbauchunken besitzen einen gedrungenen Körper, der nicht ganz so stark abgeflacht ist wie bei der verwandten Rotbauchunke (Bombina bombina), sowie eine gerundete Schnauze. Die Pupille ist herzförmig, das Trommelfell ist äußerlich nicht erkennbar. Die Oberseite weist zahlreiche Warzen mit erhabenen schwarzen Hornstacheln auf.
Aufgrund der phylogenetischen Position und der interessanten Fortpflanzungsbiologie (einschließlich Bastardisierung, siehe unten) ist die Genetik der Gelbbauchunke von Interesse.[5] Erste Ergebnisse eines Genomprojektes deuten auf ein Genom von ca. 4,7 GB hin, also eine Genomgröße, die weit über der des Humangenoms liegt.[6] Die Genomsequenz dürfte die weitere Analyse der Evolution und Biologie der Gattung Bombina und ihrer Verwandten vorantreiben.
Die Gelbbauchunke ist ein Bewohner des Berg- und Hügellandes im mittleren und südlichen Europa. Im Einzelnen reicht die Verbreitung von Frankreich über Belgien, die Südspitze der Niederlande (Limburg), Süd- und Mitteldeutschland, die Schweiz, Österreich, Italien nördlich des Po (weiter südlich findet sich die Apennin-Gelbbauchunke), Tschechien, Slowakei, den äußersten Südrand Polens, Rumänien, Bulgarien, die Staaten des früheren Jugoslawien und Albanien bis nach Griechenland. In den Mittelgebirgslagen Mittel- und Süddeutschlands, aber auch in der Oberrheinebene, ist sie zwar recht verbreitet, dabei vielerorts aber nur noch in zerstreuten Populationen vorhanden. Die nördliche Grenze der aktuellen Gesamtverbreitung befindet sich im niedersächsischen Weser-Leinebergland (Landkreis Schaumburg).[7], siehe dazu auch die Verbreitungskarte des BfN[8].
Im Osten und Süden des Verbreitungsgebietes (z. B. Tschechien, Ost-Österreich, nördliche Balkanhalbinsel) überschneidet sich das Areal der Gelbbauchunke teilweise mit dem der Rotbauchunke. Hier kann es gelegentlich zur Bastardierung zwischen beiden Arten kommen, wobei die resultierenden Hybriden Merkmale beider Elterntiere haben.
Neben der Apennin-Gelbbauchunke (Bombina pachypus), deren Artstatus umstritten ist, die aber zumindest als Unterart gesichert ist, gibt es noch die Griechische Gelbbauchunke (Bombina variegata scabra Küster, 1843), die auf der Balkanhalbinsel (u. a. Griechenland, Albanien, Bulgarien, Nordmakedonien, Montenegro) verbreitet ist. Eine weitere, jedoch stark umstrittene, Unterart vom Balkan ist die Dalmatinische Gelbbauchunke (Bombina variegata kolombatovici Bedriaga, 1890).[9]
Die Gelbbauchunke gehört zu den Amphibien mit einer engen Gewässerbindung. Ursprünglich war die Art ein typischer Bewohner der Bach- und Flussauen. Sie besiedelte hier die in Abhängigkeit von der Auendynamik immer wieder neu entstehenden, temporären Kleingewässer. Auch in ihren zivilisatorischen Ersatzbiotopen bevorzugt sie temporär wasserführende Klein- und Kleinstgewässer auf lehmigem Grund, wie Traktorspuren, Pfützen und kleine Wassergräben. Meist sind diese vegetationsarm und frei von konkurrierenden Arten und Fressfeinden. Durch die schnelle Erwärmung der Gewässer ist eine rasche Entwicklung des Laichs und der Larven gewährleistet. Man findet diese Pionierart heute überwiegend in Steinbrüchen, Lehm- oder Kiesgruben sowie auf Truppenübungsplätzen.
Die große Mobilität der Jungtiere begünstigt die spontane Besiedlung von neu entstehenden Lebensräumen. An Land suchen die Tiere Verstecke unter Steinen, Totholz und in Lücken- und Spaltensystemen von Felsen auf. Vorwiegend dämmerungs- und nachtaktiv gehen sie auf die Jagd nach Insekten (Käfer, Ameisen, Zweiflügler u. a.). Zu ihren Fressfeinden gehören Rückenschwimmer, Ruderwanzen, Großlibellenlarven, Molche und Stichlinge (für die Kaulquappen) sowie Vögel wie Elstern und auch Amseln (für die Jung- und Alttiere).
Bei Gefahr nimmt die Gelbbauchunke manchmal die sogenannte Kahnstellung ein. Dabei macht sie ein Hohlkreuz, so dass die Ränder ihres intensiv aposematisch gefärbten Bauches und ihrer Gliedmaßeninnenseiten von oben sichtbar werden (Unkenreflex). Dies soll Fressfeinde vor dem Hautgift warnen, das sie in dieser Situation absondert. In ihrem Wehrsekret wurden zwei toxische Nonapeptide identifiziert.[10] Für den Menschen ist das Gift nicht gefährlich, aber stark schleimhautreizend.
Die Paarungsrufe der Männchen hört man im Spätfrühling und Frühsommer als ein dumpfes, aber melodiöses „uh … uh … uh“. Da die Art im Gegensatz zur Rotbauchunke keine Schallblasen hat, sind die Rufe nur recht leise. Die Lautfolgen werden mehr als 40-mal pro Minute wiederholt und damit deutlich zahlreicher als bei der Rotbauchunke. Ruf- und Laichaktivitäten (bis zu drei Perioden im Jahr) werden häufig durch ergiebige Regenfälle stimuliert, weil oft erst dann die bevorzugten Kleinstgewässer zur Verfügung stehen. Die Männchen klammern die Weibchen nicht hinter den Vorderbeinen wie etwa bei den Echten Kröten oder den meisten Fröschen, sondern in der Hüftregion.
Die Eier werden von dem Paar in lockeren Klümpchen von 2 bis 30 Eiern an untergetauchte Grashalme und ähnliche Strukturen geheftet; insgesamt kann ein Weibchen 120 bis 170 Eier jährlich produzieren. Die Eier sind auf der Oberseite mittelbraun, am unteren Pol hellbraun und haben einen Durchmesser von 1,5 bis zwei Millimetern, die Gallerthüllen von fünf bis acht Millimetern. Die Hauptlaichzeit reicht in Mitteleuropa von Mai bis Juni.
Der Schlupf der Kaulquappen erfolgt bereits nach zwei bis drei Tagen. Der obere Flossensaum der zuletzt maximal 55 Millimeter langen älteren Larven reicht höchstens bis zur Rumpfmitte; das Ende des in Relation zum Rumpf recht kurzen Schwanzes ist abgerundet. Die Tiere haben eine schmutzig graue Grundfarbe. Die Dauer der Larvenentwicklung hängt von der Umgebungstemperatur ab und liegt meist zwischen 41 und 67 Tagen. Die umgewandelten Metamorphlinge (Jungunken) haben dann eine Länge von 12 bis 16 Millimetern. Nach ein bis zwei Überwinterungen erreichen Jungtiere die Geschlechtsreife und nehmen selbst am Fortpflanzungsgeschehen teil. In Gefangenschaft wurde eine Unke 27 Jahre alt.
Eine Gefährdung für die Vorkommen der Gelbbauchunke geht vor allem von Lebensraumverlusten aus, wie sie beispielsweise durch das Verfüllen von Tümpeln, durch Ausbau von unbefestigten Waldwegen und Rückegassen, aber auch durch natürliche Sukzession (vor allem die Verbuschung) der Pionierbiotope auftreten. Infolge einer räumlichen Verinselung, also einer Fragmentierung der Habitate (beispielsweise durch Straßen oder intensive Landwirtschaft), werden Vorkommen voneinander getrennt. Dadurch werden der genetische Austausch zwischen den Populationen und die Zuwanderung von außen eingeschränkt, was letztlich die Überlebensfähigkeit der isolierten Bestände gefährdet.
Gesetzlicher Schutzstatus (Auswahl)[11]
Nationale Rote Liste-Einstufungen (Auswahl)[13]
Um kleine Bestände zu unterstützen, können künstliche Reproduktionsgewässer, wie etwa eingegrabene, aus Beton gegossene Becken, helfen. Diese werden in einem schmalen Streifen entlang eines Grabens oder Baches eingebaut. Untersuchungen zeigten, dass die künstlichen Kleingewässer bereits nach wenigen Tagen von den Unken angenommen wurden und den ganzen Sommer über besetzt blieben sowie zum Laichen genutzt wurden.[14]
Die Gelbbauchunke (Bombina variegata), auch Bergunke genannt, gehört innerhalb der Klasse der Amphibien zur „urtümlichen“ Familie Bombinatoridae (in vielen Übersichten wird sie aber noch zu den Scheibenzünglern gestellt) und zur Gattung der Unken. Der kleine, spitzwarzige Froschlurch hat eine unscheinbar gefärbte Oberseite, während die Bauchseite eine leuchtend gelbe Warnfärbung aufweist. Die Art kommt regional auch in Mitteleuropa vor und bevorzugt als Lebensraum lehmige Pfützen und Kleintümpel.
Die Gelbbauchunke wurde von der Deutschen Gesellschaft für Herpetologie und Terrarienkunde zum Lurch des Jahres 2014 gekürt.
Η κιτρινομπομπίνα, Bombina variegata (Linnaeus, 1758) είναι ένας φρύνος της οικογένειας Bombinatoridae. Πρόκειται για ένα μικρό φρύνο με ολικό μήκος που συνήθως δεν ξεπερνά τα 5 cm[1]. Συναντάται σε ρηχά νερά, όπως λιμνούλες, ρεματιές, μικρά ποτάμια, ακόμα και σε περιστασιακά γεμάτες με νερό λακκούβες. Προτιμά συνήθως μεγαλύτερα υψόμετρα από την κοκκινομπομπίνα και μπορεί να παρατηρηθεί ακόμα και σε ύψος 2000 m[2].
Απαντάται στη δυτική, κεντρική και νοτιοανατολική Ευρώπη, συμπεριλαμβανομένης της Ιταλικής χερσονήσου (απουσιάζει από τη Σικελία). Στην Ελλάδα εξαπλώνεται σε όλο τον ηπειρωτικό κορμό, ενώ απουσιάζει από την Πελοπόννησο[1].
Κυρίως ημερόβιος φρύνος παρόλο που δραστηριοποιείται συχνά και τη νύχτα. Τρέφεται κυρίως με έντομα και προνύμφες αυτών. Τα θηλυκά γεννούν αρκετές φορές ανά εποχή, 120-170 αυγά συνολικά[2].
Όταν συλληφθεί, καμπυλώνει χαρακτηριστικά το σώμα και τα άκρα του προς τα πάνω, επιδεικνύοντας τα έντονα χρώματα της κοιλιάς του, προειδοποιώντας έτσι για το τοξικό υγρό που εκκρίνει μέσω αδένων του δέρματος σε περίπτωση άμυνας. Οι ουσίες αυτές, αν και αποτελεσματικές στην αποτροπή θηρευτών, είναι εντελώς ακίνδυνες για τον άνθρωπο όταν έρθουν σε επαφή με το δέρμα.
Η κιτρινομπομπίνα, Bombina variegata (Linnaeus, 1758) είναι ένας φρύνος της οικογένειας Bombinatoridae. Πρόκειται για ένα μικρό φρύνο με ολικό μήκος που συνήθως δεν ξεπερνά τα 5 cm. Συναντάται σε ρηχά νερά, όπως λιμνούλες, ρεματιές, μικρά ποτάμια, ακόμα και σε περιστασιακά γεμάτες με νερό λακκούβες. Προτιμά συνήθως μεγαλύτερα υψόμετρα από την κοκκινομπομπίνα και μπορεί να παρατηρηθεί ακόμα και σε ύψος 2000 m.
The yellow-bellied toad (Bombina variegata) belongs to the order Anura, the archaeobatrachial family Bombinatoridae, and the genus of fire-bellied toads. The toad is distributed mainly across western Europe as well as a handful of countries in eastern Europe. While the population of the toad is steadily decreasing over time, its numbers are not critical enough to be considered threatened or extinct. Conservation efforts in Germany are taking place to remedy the declining population before it is too late.
The toad is characterized by its bright ‘yellow belly,’ and has a dark brown and green dorsal body. The toad displays crypsis to camouflage itself from predators. It also positions itself to display yellow coloration when facing a threat. The warts found on the dorsal side allow for the toad's toxins to be readily excreted when needed.
The yellow-bellied toad is fascinating species to study because of its breeding choices; it chooses calculated risk when deciding to breed in shallow, unpredictable locations. Due to its breeding and egg laying behavior, climate change and habitat fragmentation heavily impact this species.
Specimens range from 28–56 mm, typically weighing between 2.3 and 12 g.[1] This places them among the smaller members of the family Bombinatoridae, which can reach sizes of 7 cm. Their top side is grey-brown, often with washed-out, bright spots. Their under side, including the inner sides of the limbs, fingers, and toes, is grey-blue to black-blue with striking, bright yellow to orange spots or patches, usually covering more than half of the underside. Yellow-bellied toads have compact bodies - though not so flat as the related European fire-bellied toad - and a rounded snout. The pupils are heart-shaped, with the eardrums not visible. The overside has numerous warts with raised swirls. A study conducted by researchers from Brill Academic Publishers had concluded that there are sexually dimorphic differences noted within the species. Males of the species have notably longer humerus length resulting in a longer forelimb length; It is believed to give them an advantage while coupling and while fighting other males of the same species. [2]
A study conducted by Bogdan Stugren and Stefan Vancea in 1968 on yellow-bellied toads in Romania and the USSR established eight different forms of B. variegata, expanding on the three forms previously posited by Michalowski in 1958.[3] Each of these forms represents a ratio of yellow to black markings on the underside of the toad, ranging from nearly completely yellow (Form 1) to nearly completely black (Form 8). Stugren and Vancea found that the undersides of B. variegata specimens from northern regions typically had greater coverage by black markings than those that were found in southern regions.
The yellow-bellied toad is found in mountainous regions, typically in Western Europe. Within Europe, two species of Bombina exist, Bombina variegata and Bombina bombina. Due to postglacial advance of the latter, Bombina variegata has been found in lower numbers in comparison. The yellow-bellied toad is also found in a much smaller, more isolated, region. France, Germany, Belgium, and the Netherlands are the most common locations in which the toad would be found. Due to habitat disturbances, the areas of occupancy for the yellow-bellied toads have seen a significant decrease in size.[4]
Factors associated with climate change, including habitat loss, loss of genetic variation and increase in disease spread have all greatly contributed to the decline of the Yellow-bellied toad.[5] It is important to obtain accurate information about the exact issues plaguing the population at a local, regional, and continental scale. Each level requires a different solution and multiple conservation efforts must be performed to get the species outside of endangered. The species has been largely isolated in recent years due to habitat complications, the largest of which is fragmentation. The reduced genetic diversity can arise from the known habitat fragmentation or the result of post-glacial dispersal, resulting in high levels of inbreeding. In populations that are affected by both, the decline in genetic diversity is evident. Current conservation efforts must focus on the improvement of habitat in an effort to increase genetic diversity.[5]
The yellow-bellied toad is endangered in Germany. Experiments have been done in an attempt to increase the current population by moving individuals in higher density areas to areas with low populations of the frog. Due to this movement, the ability of the frog to adapt its coloration to suit the environment they are placed in is critical to their survival. Variation in coloration plasticity amongst individuals in the species forces researchers to consider assessing an individual’s ability to change coloration prior to relocation.[6] Another issue arising with the relocation of some individuals to another habitat is the spread of disease that can come with it.[5] Ensuring individuals of the species have a better chance of interaction would increase the negative effects habitat fragmentation has had. Therefore, on a continental scale, conservation efforts should focus on the creation of metapopulations as a counteractive mechanism, allowing for more interactions to take place and increasing variation through breeding.[5]
Female yellow-bellied toads have the ability to produce offspring multiple times each mating season and long-lived individuals are possible. However, to find a female actually producing offspring multiple times per year is rare. Female reproductive output is also very low, having the capacity to lay over 200 eggs at a given time, but typically seen to only lay about 40.[7] This is because there is little incentive to produce offspring in conditions when adult survival is high and offspring have a more variable likelihood of survival.[7]
The life span of yellow-bellied toads encompasses the broad range of 5-23 years. Mortality rates directly determine the average lifespan. The range an individual falls in the fast-slow continuum is dependent on factors such as climate, habitat, and food availability. Climate especially plays the largest extrinsic role as it mediates the predictability of a habitat for an individual as well as the availability of breeding sites. The risk of predation is another factor that plays a large role in the life span of an individual. The yellow-bellied toad has defense mechanisms such as skin-secreting toxins that decrease its appeal to predators, allowing for a longer life span. Interestingly, in the yellow-bellied toad, specific populations exhibit a wide range of life spans across the fast-slow continuum, with climate conditions accounting for a significant amount of variation.[5]
Tadpoles develop rapidly and can reach 55mm in length. They have a blunt tail and are typically grayish-brown or, in rare cases, transparent.[1] Tadpoles and eggs are vulnerable to predation from various small pond-dwelling creatures, such as leeches, fish, and some aquatic beetles.[8] A study published in 2016 in the Canadian Journal of Zoology indicated that tadpoles in warmer water develop more quickly than those in cooler climates, meant to mimic the differing environments found in forested areas and sunny quarries.[9]
To maximize mating for a male, some yellow-bellied male toads will engage in water-wave-producing behavior. This is where a male will kick its hind legs into a small body of water, generating a wave-like pattern. This pattern not only attracts females but is a mechanism of making a male’s territory known. Since yellow-bellied toads have very specific, typically risky, breeding sites, having a territory is very important since the highest chance of offspring survival occurs ponds that last longer. Not all males can exhibit this wave-generating behavior because it is exclusive to ponds of a specific depth.[10]
In the instance where the owner of a territory comes into contact with an intruder, the owner will move towards the intruder and engage in a fight. The fight consists of each male trying to climb the other’s back, with the winner eventually holding the other frog down through its legs while climbing its back. The loser immediately swims away while the winner begins exhibiting wave-producing behavior at very high frequencies, marking its territory.[10]
The yellow-bellied toad has the ability to breed in unpredictable habitats and locations, including shallow pools that have the ability to disappear overnight. Within the Bombinatoridae family, the yellow-bellied toad is the only species that chooses to breed in such unpredictable sites.[11]
The yellow-bellied toad lays eggs in ponds of a particular temperature and duration. When given the choice between a warm pond, or a cooler one, the frog will lay its eggs in the warmer pool because of heat being conducive for healthy egg growth and development. Therefore, laying in warmer ponds increases the reproductive fitness of the frog.The frog would also prefer ponds that persist for an intermediate period of time because laying eggs in a pond that persists for a long time risks the introduction of a large number of predators to the eggs while short-lived ponds have too few as well as carrying the risk of desiccation. A key component of site selection is the ability for rapid development to occur. Site selection and rapid development are key to survival because most deaths occur at this stage.[5] It was found that pond duration, rather than risk of predation is the most critical factor to site selection. Pond desiccation, unlike predation, has the ability to kill an entire group of tadpoles or eggs.[12]
The frog’s displays a darker brown or green coloration on its dorsal body allowing the species to participate in crypsis, thereby giving the frog a camouflage effect against prospective predators.[6] The yellow bellied toad also displays aposematism in its ventral body with varying shades of yellow displayed as a warning signal to predators of its poisonous skin.[6] Different individuals in the yellow-bellied toad species display variations of the darker dorsal and yellow ventral body, depending on their specific location. When placed in lighter or darker environments the frogs are also able to alter the shade of their coloration in an attempt to better disguise themselves. There is a natural variation in coloration amongst the species, with some individuals having a brighter coloration. It was found that these individuals adapted to enhance their crypsis, for example covering themselves with pond soil, suggesting an awareness that their dorsal body does not conceal them perfectly in comparison to their environment.[6] This ability to rapidly change coloration when moving to lighter or darker environments is achieved by the movement of melanosomes, or pigment containing vesicles, to different parts of the cell.[6] The ability to alter the shade of coloration is very important in reducing the amount of time the frog is vulnerable to predators as the longer they stand out amongst other individuals in the species, the higher the risk of predation is.[6][[Image:Bombina variegata1.jpg|thumb|220px|A pair of yellow-bellied toads in amplexus. The warts present on the dorsal side of the yellow-bellied toad allow for an opening of venom glands when threatened. The difference in coloration on the cryptic dorsal side and bright yellow ventral body allow for the yellow-bellied toad to remain camouflaged most of the time, only flashing its coloration under duress. Escape, full, and partial threat responses are the most commonly seen among yellow-bellied toads. The toad was also seen to puff up their chest, discouraging predators who prefer to capture and swallow their prey at once. Immobility is the most passive of responses, with the toad remaining still in an attempt to conceal itself as much as possible, avoiding confrontation entirely. While the toxin of the yellow-bellied toad is not fatal to humans, it can cause significant discomfort to most animals and is fatal to smaller ones.[13]
The difference in what type of defense mechanism is used by yellow-bellied toads varies significantly among populations, even more so than species. The differences in predators among the populations is responsible for this difference. If one individual encounters snakes more often, it will employ the defense of puffing up more often than individuals that have never encountered a snake.[13]
{{cite journal}}: CS1 maint: multiple names: authors list (link) Database entry includes a range map and justification for why this species is of least concernThe yellow-bellied toad (Bombina variegata) belongs to the order Anura, the archaeobatrachial family Bombinatoridae, and the genus of fire-bellied toads. The toad is distributed mainly across western Europe as well as a handful of countries in eastern Europe. While the population of the toad is steadily decreasing over time, its numbers are not critical enough to be considered threatened or extinct. Conservation efforts in Germany are taking place to remedy the declining population before it is too late.
The toad is characterized by its bright ‘yellow belly,’ and has a dark brown and green dorsal body. The toad displays crypsis to camouflage itself from predators. It also positions itself to display yellow coloration when facing a threat. The warts found on the dorsal side allow for the toad's toxins to be readily excreted when needed.
The yellow-bellied toad is fascinating species to study because of its breeding choices; it chooses calculated risk when deciding to breed in shallow, unpredictable locations. Due to its breeding and egg laying behavior, climate change and habitat fragmentation heavily impact this species.
El sapo de vientre amarillo (Bombina variegata) es una especie de anuro de la familia Bombinatoridae.[2]
Los adultos de mayor tamaño no llegan a 35 mm (machos) o 55 mm (hembras), siendo por tanto una de las especies más pequeñas de Archaeobatrachia. Su dorso es marrón-verdoso, frecuentemente con manchas brillantes. El vientre, incluido la cara interna de los brazos y los dedos, son de un tono gris-azulado a negro-azulado con conspicuas manchas amarillo-anaranjadas que cubren la mitad de dicha superficie. Estos anuros tienen un cuerpo compacto no tan aplanado como Bombina bombina. Las pupilas son acorazonadas sin tímpanos visibles, los laterales tienen numerosas verrugas.
El canto de apareamiento de los machos se oye durante la primavera tardía y verano temprano. Como esta especie no tienen sacos bucales, el canto es suave.
Puesta: Los huevos aparecen desde mayo hasta junio; se disponen en paquetes laxos de 2 a 30 huevos en la hierba u otra vegetación. Tienen un color marrón medio por la cara superior, y marrón brillante en la cara inferior. El tamaño medio es de 1,5 a 2 mm, con una capa mucosa de 5-8 mm.
Larvas: Tienen un tamaño máximo de 55 mm, con el final de la cola redondeado. Son de un color gris sucio.
Es una especie estrechamente asociada al agua. Originariamente vivía típicamente a lo largo de arroyos y ríos, dependiendo de la disponibilidad de agua. Bajo la influencia humana su hábitat sigue dependiendo de la disponibilidad de pequeños cuerpos de agua en tierra fangosa, como roderas de tractores, charcos, y zanjas. La mayoría de estas zonas son ricas en vegetación y libres de depredadores y especies competidoras. El calentamiento de estos pequeños cuerpos de agua asegura el desarrollo rápido de embriones y larvas. La elevada movilidad de los juveniles permite la dispersión de esta especie a nuevas zonas adecuadas. En tierra buscan refugio debajo de rocas, madera muerta y grietas. Prosperan en zonas montañosas y colinas de Europa central y meridional como el valle alto del Rin.
Esta especie se encuentra en Europa de 100 a 2100 m de altitud en los siguientes países: Francia, Bélgica, Luxemburgo, Holanda, Alemania, Suiza, norte de Italia, Austria, Chequia, Polonia, Eslovaquia, Hungría, Eslovenia, Croacia, Bosnia-Herzegovina, Serbia, Montenegro, Albania, Macedonia del Norte, Grecia, Bulgaria, en Rumania y oeste de Ucrania.
Pareja en amplexo
El sapo de vientre amarillo (Bombina variegata) es una especie de anuro de la familia Bombinatoridae.
Bombina variegata Bombina generoko animalia da. Anfibioen barruko Bombinatoridae familian sailkatuta dago, Anura ordenan.
Bombina variegata Bombina generoko animalia da. Anfibioen barruko Bombinatoridae familian sailkatuta dago, Anura ordenan.
Vuoristokellosammakko (Bombina variegata) on kellosammakoiden sukuun kuuluva Keski- ja Etelä-Euroopassa esiintyvä sammakkolaji.
Se risteytyy usein sukulaislajinsa kellosammakon (Bombina bombina) kanssa.[1]
Vuoristokellosammakko on eurooppalainen laji, joka on yleinen Keski-Ranskassa, Saksan keskiosissa, Sveitsissä, Koillis-Italiassa, Balkanin alueella ja Karpaattien vuoristossa Itä-Euroopassa. Yksittäisiä populaatioita on havaittu myös Unkarissa, Saksan pohjoisosissa, Luoteis-Ranskassa, Luxemburgissa, ja Alankomaissa. Sitä on aiemmin tavattu myös Belgiassa ja Ranskan eteläosissa, mutta sen oletetaan sittemmin hävinneen kyseisiltä alueilta.[1]
Laji elää 100–2 100 metrin korkeudessa merenpinnan yläpuolella. Matalimmissa korkeuksissa elävien populaatioiden elinympäristöjä ovat lehtimetsät. Korkeammalla lajia tavataan havumetsissä ja aukeilla ylängöillä. Sen elinympäristöjä ovat myös sekametsät, pensaikot, niityt, tulvatasangot ja ruohotasangot. Se viihtyy kosteikoissa ja valitsee lisääntymispaikakseen yleensä lätäkön metsästä tai metsän lähettyviltä.[1]
Vuoristokellosammakko (Bombina variegata) on kellosammakoiden sukuun kuuluva Keski- ja Etelä-Euroopassa esiintyvä sammakkolaji.
Se risteytyy usein sukulaislajinsa kellosammakon (Bombina bombina) kanssa.
Bombina variegata
Bombina variegata est une espèce d'amphibiens de la famille des Bombinatoridae[1]. Il est appelé en français Sonneur à ventre jaune ou Crapaud sonneur à ventre jaune ou Sonneur à pieds épais.
Cette espèce se rencontre en Europe de 100 à 2 100 m d'altitude[1],[2] :
Cette espèce a été introduite au Royaume-Uni.
L'habitat de cette espèce est constitué de mares, ornières ou flaques d'eau en forêt.
L'espèce résiste particulièrement à un pH acide (< 7).
Ce petit crapaud mesure de 3,5 à 5,5 cm de longueur[3] ; il est reconnaissable par sa face ventrale jaune tranchant avec sa face dorsale d'un gris terne et la pupille de son œil en forme de cœur.
La face dorsale du sonneur à ventre jaune est marron-grisâtre et terne, ce qui lui assure un camouflage au sein de son habitat naturel. La face ventrale, jaune tachetée de noir, contraste fortement avec sa face dorsale. Le crapaud peut la dévoiler à un éventuel prédateur en cas de menace afin d'effrayer son agresseur.
Les sonneurs à ventre jaune (mais aussi d'autres membres de la famille), quand ils sont dérangés ou agressés, présentent un comportement défensif : c'est le réflexe d'Unken. Les animaux ainsi dérangés s'arc-boutent sur leur dos et présentent leur face ventrale à leur assaillant, tandis qu'ils rapprochent leurs membres de leur corps. Mais si l'agression continue, le sonneur peut libérer un liquide visqueux, poison irritant pour les yeux, et à l'odeur repoussante.
Il hiberne d'octobre à avril.
Bombina variegata se nourrit d'insectes, vers, petits crustacés et mollusques, et peut vivre jusqu'à 8-9 ans[4] (mais le record est de 34 ans en captivité)[réf. nécessaire].
Le sonneur à ventre jaune se reproduit à partir de 3-4 ans, en mai-juin jusqu'en été en moyenne montagne[4] ; il utilise plusieurs mares (en général temporaires) pour se reproduire[5], accrochant seulement quelques œufs (1 à 10 maximum) de façon regroupée ou isolée aux plantes aquatiques immergées. Ceux-ci éclosent après 5 jours, et les têtards se métamorphosent 34 à 131 jours après l'éclosion[4].
En France, l'espèce est protégée[6]. Les évaluations réalisées par le Comité français de l’UICN et le Muséum national d'histoire naturelle montrent que le sonneur à ventre jaune fait partie des huit espèces d'amphibiens menacées sur le territoire métropolitain (catégorie VU, « espèce vulnérable »)[7]. Un premier Plan national d'action (PNA) en faveur de l'espèce a été mis en œuvre par la région Grand-Est de 2011 à 2015[8].
En Belgique, l’espèce était sur le point de disparaître. Une des dernières populations a été sauvegardée lors de la destruction du site au milieu des années 1980 (construction du site du Sart-Tilman de l’Université de Liège) et déplacée sur un autre site proche, où elle a été aidée. Une seconde population fut découverte plus tard dans l'Entre-Sambre-et-Meuse. Depuis, un programme de réintroduction à partir de ces populations est en cours, notamment sur un terrain militaire en Famenne, et via une pisciculture à Érezée[9]. Ces programmes permettent une redéveloppement des populations[10],[11]. Également présent sur le cours de la Gueule.
Accouplement par amplexus lombaire
Bombina pachypus a été placée en synonymie avec Bombina variegata[12].
Bombina variegata
Bombina variegata est une espèce d'amphibiens de la famille des Bombinatoridae. Il est appelé en français Sonneur à ventre jaune ou Crapaud sonneur à ventre jaune ou Sonneur à pieds épais.
Bombina variegata é unha especie de anfibio anuro da familia Bombinatoridae que vive esencialmente en Centroeuropa e os Balcáns.[2]
Os adultos de maior tamaño non chegan a 35 mm de lonxitude (machos) ou 55 mm (femias), polo que é unha das especies máis pequenas de Archaeobatrachia. O seu dorso é marrón verdoso, frecuentemente con manchas brillantes. O ventre, incluíndo a cara interna dos brazos e os dedos, son dun ton gris azulado a negro azulado con conspicuas manchas amarelo-alaranxadas que cobren a metade de dita superficie, moi rechamantes e características. Estes anuros teñen un corpo compacto non tan aplanado como Bombina bombina. As pupilas son acorazonadas sen tímpanos visibles, a parte superior ten numerosas verrugas.
O canto de apareamento dos machos pode sentirse na primavera tardía e inicios do verán. Como esta especie non ten sacos bucais, o canto é suave.
Posta: Os ovos póñenos desde maio ata xuño, agrupados en paquetes laxos de 2 a 30 ovos deixados na herba ou outra vexetación. Teñen unha cor marrón pola cara superior, e marrón máis brillante na cara inferior. O tamaño medio é de 1,5 a 2 mm, cunha capa mucosa de 5 a 8 mm.
Larvas: As larvas ou cágados teñen un tamaño máximo de 55 mm, co final da cola arredondado. Son de cor cincenta sucia.
É unha especie estreitamente asociada coa auga. Orixinariamente vivía ao longo de regatos e ríos, dependendo da dispoñibilidade de auga. Baixo a influencia humana o seu hábitat segue dependendo da dispoñibilidade de pequenos corpos de auga en terra lamosa, como rodeiras deixadas por tractores, charcos, e gavias. A maioría destas zonas son ricas en vexetación e están libres de depredadores e especies competidoras. O quecemento destes pequenos corpos de auga asegura o desenvolvemento rápido de embrións e larvas. A elevada mobilidade dos xuvenís permite a dispersión desta especie a novas zonas axeitadas. En terra procuran refuxio debaixo de rochas, madeira morta e gretas. Prosperan en zonas montañosas e outeiros de Europa central e meridional como o val do alto Rhin.
Esta especie encóntrase en Europa entre os 100 e 2100 m de altitude nos seguintes países: Francia, Bélxica, Luxemburgo, Países Baixos, Alemaña, Suíza, norte de Italia, Austria, Chequia, Polonia, Eslovaquia, Hungría, Eslovenia, Croacia, Bosnia e Hercegovina, Serbia, Montenegro, Albania, República de Macedonia, Grecia, Bulgaria, Romanía e oeste de Ucraína. Está ausente de toda a península Ibérica, Galicia incluída.
Parella en amplexo
Bombina variegata é unha especie de anfibio anuro da familia Bombinatoridae que vive esencialmente en Centroeuropa e os Balcáns.
Žuti mukač (Bombina variegata) je vrsta iz porodice mukača i nastanjuje sve vrste voda stajaćica i područja oko njih širom srednje i jugoistočne Europe.
Žuti mukač je mala bezrepa zdepasta žaba. Može narasti od 35 do 55 mm. Leđa su im sivo smeđe do tamno maslinaste boje. Abdomen, uključujući i ekstremitete, je žut s crnim mrljama.
Karakteristična je zjenica žutog mukača u obliku srca.
Glasaju se u zborovima, danju i uvečer zvonkim "pup ... pup ... pup", jedan do dva zova na sekundu. Mužjaci nemaju vokalnu vrećicu (rezonator).
Jaja su im pojedinačna ili u labavim nakupinama do 30. Ličinke su jednolični smeđkasti punoglavci, a repna peraja im je posuta točkama.
Žuti mukač je aktivan preko dana i tijekom noći. Hrani se pretežno kopnenim beskralješnjacima (kukcima, gliste) koje hvata blizu vodenih staništa.
Parenje se odvija najčešće poslije kiše tijekom proljeća i ljeta. U vrijeme parenju, mužjaci privlače ženke zovom. Kad se uspiju približiti ženki, obuhvaćaju ih oko bokova prednjim nogama. Ženka ispušta jaja, a mužjak ih pritom oplođuje. U jednom ciklusu, ženka položi do 300 jaja, najčešće među vodenu vegetaciju, ali i slobodno na dno. Punoglavci koji se iz njih izlegu narastu do 45 mm, a krajem ljeta i početkom jeseni se preobraze u mukače dugačke 10-15 mm. Spolnu zrelost dostižu sa 2 do 4 godine, a ženkama se to događa kasnije od mužjaka. Mogu doživjeti 12 godina u prirodi, a u zatočeništvu i do 20.
Parenje žutog mukača amplexus
Žuti mukač je vodena vrsta. Živi u brdovitim i planinskim predjelima, u vodenim staništima, a može ih se naći čak i u malim lokvama na brdskim cestama.
Živoni prostor obuhvaća zapadnu, središnju i jugoistočnu Europu. Države u kojima ih se može naći su Ukrajina, Moldavija, Rumunjska, Bugarska, Grčka, Albanija, Makedonija, Srbija, Crna Gora, Hrvatska, Mađarska, Slovačka, Poljska, Italija, Slovenija, Švicarska, Austrija, Njemačka, Češka, Francuska, Luksemburg i Belgija.
Ličinke su biljojedi, te se hrane algama i vodenim biljem.
Odrasle jedinke na kopnu love puževe, stonoge, kukce i ličinke kukaca. Povremeno se hrane i u vodi, uglavnom račićima, vodenim kolutićavcima, kukcima, ličinkama kukaca.
Ličinke žutog mukača su hrana vodenim kukcima (ličinkama i odraslim jedinkama), vodenjacima, gmazovima, pticama i malim sisavcima.
Preobražene mukače štiti koža koja luči otrovne tvari koje ih čine nejestvima za mnoge vrste. Kada su napadnuti, često pokazuju boje koje signaliziraju da su otrovni. To rade uvrtanjem ili preokretanjem, pokazujući jarko obojen trbuh i druge obojene dijelove.
Bombina variegata je zaštićen Bernskom konvencijom (Appendix II, strogo zaštićena vrsta) i europskom direktivom o zaštiti staništa i vrsta (Annex II, IV).
Žuti mukač može se naći u Turopolju i na popisu je zaštićenih vrsta u Republici Hrvatskoj. Štiti ga Pravilnik o proglašavanju divljih svojti zaštićenim i strogo zaštićenim (NN 07/06), gdje je naznačen kao "strogo zaštićena svojta".
Žuti mukač (Bombina variegata) je vrsta iz porodice mukača i nastanjuje sve vrste voda stajaćica i područja oko njih širom srednje i jugoistočne Europe.
L'ululone dal ventre giallo (Bombina variegata Linnaeus, 1758) è un anfibio anuro appartenente alla famiglia Bombinatoridae.[2]
Il suo nome deriva, oltre che dal colore del ventre, dal tipico canto che emette nel periodo riproduttivo, costituito da un "uuh... uuh... uuh...", ripetuto anche più di 40 volte al minuto.
La sua lunghezza massima è di 5 cm e può raggiungere i 20 anni di vita. Se viene disturbato si difende secernendo una sostanza biancastra volatile irritante per le mucose.
Una specie simile è l'ululone dal ventre rosso (Bombina bombina) che differisce per il colore ed è presente nell'Europa centro-orientale fino agli Urali e all'Asia minore.
Diffuso in buona parte dell'Europa, Italia compresa.
Va segnalato che secondo alcuni autori Bombina pachypus (ululone appenninico), in seguito a studi genetici effettuati sul DNA mitocondriale, è considerato un sinonimo di B. variegata.[2][3]
L'ululone dal ventre giallo (Bombina variegata Linnaeus, 1758) è un anfibio anuro appartenente alla famiglia Bombinatoridae.
Il suo nome deriva, oltre che dal colore del ventre, dal tipico canto che emette nel periodo riproduttivo, costituito da un "uuh... uuh... uuh...", ripetuto anche più di 40 volte al minuto.
De geelbuikvuurpad (Bombina variegata) is een padachtige kikker uit de familie Bombinatoridae en het geslacht vuurbuikpadden.[2]
De kikker heeft een groot verspreidingsgebied in het midden en zuiden van Europa en komt onder andere voor in België en Nederland. Hier is de soort echter zeer zeldzaam en ernstig bedreigd.
De geelbuikvuurpad is een kleine, gedrongen kikker met een afgeplat lichaam. De lichaamslengte is ongeveer 35 tot 45 millimeter, maximaal 56 mm, de mannetjes blijven iets kleiner dan de vrouwtjes.
De kleur van de bovenzijde is variabel, van geelbruin tot bruin, olijfgroen of grijs. De kleur verschilt enigszins per leefgebied. Zowel de voor- als achterpoten zijn donker gebandeerd, maar door de donkere basiskleur is dit moeilijk te zien. Soms komen op de rug twee vage lichte vlekken voor. Door de wratachtige structuren en de bruine tot grijze kleur van de bovenzijde van de poten, is de kikker goed gecamoufleerd en lijkt hij sprekend op een kluit. De buikzijde is juist felgeel tot oranje. Minder dan 50% van het huidoppervlak bestaat uit zwarte, ronde strepen tot vlekken die per individu in aantal, grootte en vorm kunnen verschillen. Er is echter variatie; sommige exemplaren zijn helemaal geel of juist zwart aan de onderzijde. Bij de meeste exemplaren overheerst de gele kleur en vloeien de gele vlekken van de onderzijde van de armen en de borst in elkaar over, evenals de vlekken onder de achterpoten en de liesstreek. Ieder individu heeft na het eerste levensjaar een uniek, onveranderlijk buikpatroon, het is als het ware de vingerafdruk van de kikker. Dit kenmerk wordt gebruikt bij onderzoek naar populaties en monitoring. De zwarte delen aan de onderzijde hebben hier en daar een lichter puntje, dit is een belangrijk verschil met de roodbuikvuurpad die vele witte puntjes heeft.
De geelbuikvuurpad heeft geen duidelijk zichtbare parotoïden, de gifklieren achter de ogen die andere inheemse kikkers en padden wel hebben, zoals de gewone pad. Op de rug is echter een dichte opeenhoping van vele wratachtige structuren aanwezig die bestaan uit huidklieren. Deze hebben de taak de huid vochtig te houden maar produceren ook een sterk gif dat, als het in de ogen of in de slijmvliezen komt, tot hevige pijnen kan leiden.[3] Opvallend zijn de verhoornde stekeltjes op de huidklieren, hierdoor voelt de huid van de kikker zeer ruw aan. Ook andere vuurbuikpadden hebben dergelijke structuren maar de verharde delen zijn stomper waardoor de huid veel gladder aanvoelt (roodbuikvuurpad).
De vuurbuikpad heeft geen zichtbare trommelvliezen, de ogen zijn wat meer aan de bovenzijde van de kop gepositioneerd, wat een aanpassing is op de aquatische levenswijze. De iris is geelbruin gekleurd en heeft geen goudglans maar is onopvallend. Kenmerkend is de hart- tot druppelvormige pupil, een dergelijke vorm komt maar bij weinig andere kikkers voor. Een ander verschil met veel kikkers is het ontbreken van een kwaakblaas bij de mannetjes.
De geelbuikvuurpad is in Nederland en België niet te verwarren met andere soorten door de gele buik. In Europa komt ook de roodbuikvuurpad (Bombina bombina) voor, die een westelijker verspreiding heeft. Deze soort komt niet in zuidelijk Europa voor maar meer rond de Balkan en zuidelijk Rusland tot in Azië. Het verspreidingsgebied overlapt in delen van Duitsland en Polen. De roodbuikvuurpad heeft een meer rode buik maar er is een kleuroverlap met de geelbuikvuurpad. Een belangrijk verschil is de slankere bouw van de roodbuik, en het voorkomen van vele witte puntjes op de donkere delen van de buik. Daarnaast mist de roodbuik de puntige, verhoornde stekeltjes op de wratten.
De geelbuikvuurpad is endemisch in Europa en leeft in grote delen van centraal- en zuidelijk Europa, met uitzondering van het Iberisch Schiereiland, delen van de Balkan en rond de poolgrens. In veel streken is de soort zeldzaam. De kikker komt voor in België, Bulgarije, Duitsland, Frankrijk, Griekenland, Hongarije, Italië, Liechtenstein, Luxemburg, Moldavië Montenegro, Nederland, Oekraïne, Oostenrijk, Polen, Roemenië, Servië, Slowakije, Slovenië, Tsjechië en Zwitserland. In Groot-Brittannië komen van nature geen geelbuikvuurpadden voor, hier is de soort geïntroduceerd.[4]
De populaties van de geelbuikvuurpad die ten zuiden van de Povlakte in Italië voorkomen, werden lange tijd als een aparte soort gezien; Bombina pachypus. Tegenwoordig is deze status weer teruggedraaid.
In zuidelijk Rusland tot in delen van Azië komt de Koreaanse vuurbuikpad (Bombina orientalis) voor, die meestal een groene kleur aan de bovenzijde heeft en makkelijk is te onderscheiden. Andere vuurbuikpadden komen alleen voor in Azië, zoals Bombina lichuanensis uit China en Bombina maxima uit China en Vietnam.
In Nederland komt de geelbuikvuurpad alleen nog voor in Zuid-Limburg. De kikker trekt voor de voortplanting naar liefst tijdelijke wateren; warme, ondiepe, niet-begroeide waterpartijen die veelal snel uitdrogen. De metamorfose is hierop aangepast door een zeer snelle ontwikkeling van ei tot kleine kikkertjes binnen acht weken.
In Vlaanderen zou de geelbuikvuurpad uitgestorven zijn.[5]
De geelbuikvuurpad leeft voornamelijk in natuurlijke overstromingszones van beek- en rivierdalen. Ook gecultiveerde biotopen zijn geschikt, zoals militaire oefenterreinen, plassen in bospaden, natte delen in weilanden, kleinschalige agrarische landschappen, afgravingen en industriegebieden.[6]
Net als de rugstreeppad is de geelbuikvuurpad een typische pionierssoort die permanente (visrijke) wateren mijdt en zich in de kleinste plasjes voortplant. Dit kunnen ondergelopen graslanden zijn, tot overstroomde uiterwaarden maar ook met water gevulde bandensporen zijn een geschikte afzetplaats voor de eieren. Meestal bestaan de voortplantingswateren uit ondiepe, door de zon beschenen en snel opwarmende plassen, waardoor een snelle ontwikkeling van de larven mogelijk is. De waterkwaliteit speelt geen grote rol; de kikkers worden ook in troebel of zeer voedselrijk water aangetroffen.
In Nederland gebruikt de kikker de zuidhellingen van het Limburgse Heuvelland als alternatief, evenals door de mens aangepaste landschappen als kalksteengroeves.
Gedurende de voortplantingstijd is de kikker zowel nacht- als dagactief, in de wintermaanden meer schemer- en nachtactief, alleen na een regenbui zijn de kikkers overdag weleens te zien.
In vergelijking met andere padachtige kikkers is de geelbuikvuurpad een waterminnende soort die voornamelijk in of in de directe nabijheid van het water wordt aangetroffen. Alleen de juvenielen zijn tot meer dan een kilometer ver van het water te vinden zodat ze zich naar nieuwe gebieden kunnen verspreiden.[6] Buiten de voortplantingstijd leeft de kikker echter op het land en wordt aangetroffen onder stenen, houtblokken en in struiken. De winterslaap, die loopt van september tot maart, wordt altijd op het land doorgebracht. In gebieden waar het in de zomer erg droog is, wordt een aestivatie gehouden, een zomerrust waarbij de dieren zich terugtrekken.
De voortplantingstijd loopt van april tot augustus, er zijn meerdere afzetperiodes mogelijk die niet synchroon lopen maar gedurende de lente en zomer kunnen plaatsvinden. Dit heeft waarschijnlijk te maken met de ontwikkeling van de larven in tijdelijke wateren. Doordat deze wateren snel opdrogen, komt het voor dat de larven uitdrogen voordat ze hun ontwikkeling hebben voltooid waardoor ze sterven. Ook kunnen de larven die later in het jaar zijn afgezet, verrast worden door de vorst wat ze niet overleven. Het voordeel van tijdelijke wateren is het ontbreken van concurrerende amfibieën en vissen die het legsel of de larven eten.
De mannetjes hebben geen kwaakblaas en produceren een relatief zacht geluid dat het meest lijkt op oenk - oenk - oenk, ze kwaken meestal drijvend in het water. Als een andere kikker in de buurt komt, wordt deze door het wellustige mannetje besprongen waarbij weleens per ongeluk een ander mannetje wordt gegrepen waarna deze met kwakende geluiden protesteert. Indien zich een vrouwtje aandoet, vindt de amplexus plaats, waarbij het mannetje zich met zijn voorpoten aan de lendenen van het vrouwtje vastklemt. Dit wordt de amplexus lumbaris genoemd, deze vorm van paargreep komt voor bij de meer primitieve kikkers. Pas nadat het vrouwtje haar eitjes heeft afgezet en het mannetje deze heeft bevrucht - er vindt dus geen inwendige bevruchting plaats - zit zijn taak erop en laat het mannetje los.
De eitjes worden in kleine groepjes van enkele tot enkele tientallen afgezet tegen ondergedoken plantendelen als takken en bladeren. Jaarlijks kan een vrouwtje ongeveer 120-170 eitjes produceren. De ontwikkeling verloopt relatief snel; al na twee tot drie dagen is het embryonale stadium doorlopen en kruipen de larven uit het ei. De kikkervisjes zijn dan zo'n 7 tot 9 millimeter lang en groeien in een periode van 6 tot 10 weken uit naar een lengte van ongeveer 55 mm waarna de metamorfose plaatsvindt. Net gemetamorfoseerde exemplaren hebben een lengte van ongeveer 12 tot 16 mm.[6] Na de metamorfose duurt het meestal twee jaar voordat het juveniel volwassen is, in zeldzame gevallen al na één jaar.
Van een in gevangenschap gehouden exemplaar is bekend dat een leeftijd van maar liefst 27 jaar kan worden bereikt, maar in de natuur wordt een dergelijke leeftijd door natuurlijk verval en predatie nooit gehaald.
De geelbuikvuurpad leeft van kleine ongewervelden zoals insecten en hun larven, vooral kevers, mieren en tweevleugeligen. Ook andere insecten als vlinders en andere ongewervelden als spinnen, duizendpotigen en kleine kreeftachtigen worden gegeten. In tegenstelling tot de roodbuikvuurpad worden prooien vooral op het land gevangen, ook de in het water levende kreeftachtigen worden vaak op de oever gegeten.[7]
De larven leven voornamelijk van algen, uit een onderzoek naar de uitwerpselen van larven uit Beieren bleek de mest vooral draadalgen, groenalgen en kiezelwieren te bevatten, naast zand- en modderdeeltjes.[6]
De volwassen pad heeft vooral te vrezen van vogels zoals de merel en de ekster. De larven worden gegeten door waterinsecten als ruggenzwemmers, in het water levende insectenlarven als de larve van de libel en kleine gewervelden als vissen en in het water levende salamanders.
Als een exemplaar wordt aangevallen, worden de poten tot boven het lichaam gekromd zodat de felle kleur van de randen van de buik en onderzijde van de poten zichtbaar wordt. De kikker draait zich dus niet op de rug. Vrijwel alle andere soorten kikkers en padden beschermen de kwetsbare buikzijde juist bij verstoring. Dit paradoxale gedrag wordt ook wel het unkenreflex genoemd naar het Duitse woord Unke, dat vuurbuikpad betekent en is afgeleid van het lokgeluid van de mannetjes.
Bij gevaar wordt een witte, bittere afscheiding uitgescheiden door de huid, die sterk ruikt en de slijmvliezen irriteert. De afscheiding bevat verschillende verbindingen, waaronder tryptofanen en peptiden die alleen bij vuurbuikpadden voorkomen en bombesinen worden genoemd. Ze hebben een eetlustremmende werking.[8]
Bij verstoring op het land duikt de kikker het water in, zwemt naar de bodem en verstopt zich in de modder. Bij aanraking wordt door de mannetjes een kwakend afweergeluid gemaakt.
De geelbuikvuurpad is niet overal bedreigd, in sommige streken komt de soort nog in vrij hoge aantallen voor en is nog algemeen. Een voorbeeld zijn delen van de Karpaten, waar deze soort de meest algemene amfibie is.[7] Het speciale milieu dat de geelbuikvuurpad vereist wordt echter steeds zeldzamer. Het door landschapsverandering of verdroging verdwijnen van tijdelijke poelen dwingt de kikker om de eitjes in permanente wateren af te zetten, waar roofdieren als libellenlarven, vissen of salamanders wel raad weten met de kikkervisjes. Ook het gebruik van pesticiden in de landbouw werkt de kikker tegen; de groei van zowel de eitjes als de larven wordt er negatief door beïnvloed. Ook verstoren pesticiden de algen- en bacteriëngroei in het water; een belangrijke voedselbron van de kikkervisjes.
In Nederland komt de kikker slechts in een zeer beperkt deel van Limburg voor en staat op de Nederlandse rode lijst te boek als ernstig bedreigd. In België wordt de geelbuikvuurpad zelfs beschouwd als nagenoeg uitgestorven. In Nederland gaat de kikker al decennia achteruit, in 1964 waren er ongeveer 80 vindplaatsen, in 1975 nog 19.[9] Voor 2000 kwamen ook populaties voor in Crapoel en Slekkendel maar hier is de soort uitgestorven. De geelbuikvuurpad staat in Nederland op de rode lijst als ernstig bedreigd. Tegenwoordig wordt de geelbuikvuurpad in Nederland alleen vertegenwoordigd door vijf populaties in Limburg, met een geschat aantal van zo'n 250 exemplaren (2006). De kikker komt nog voor in 't Rooth, Julianagroeve, Gerendal, Berghofwei en Wahlwiller. Hiervan herbergt 't Rooth zo'n 80% van alle exemplaren.[9]
Om de soort voor uitsterven te behoeden worden regelmatig tellingen uitgevoerd door werkgroepen als het Platform Geelbuikvuurpad en Vroedmeesterpad om de status te monitoren. Daarnaast zijn er op twee plaatsen larven uitgezet in de hoop een nieuwe populaties te vestigen. In de Groeve Blom bij Terblijt zijn vanaf 2005 1289 larven uitgezet evenals 8 gemetamorfoseerde exemplaren.[10] Ook bij de Meertensgroeve bij Vilt zijn exemplaren uitgezet. Alle uitgezette exemplaren zijn in gevangenschap opgekweekt.
De geelbuikvuurpad werd in 1758 door Linnaeus beschreven als Rana variegata. De soortnaam variegata betekent gevarieerd. Het geslacht Rana wordt tegenwoordig tot de echte kikkers (Ranidae) gerekend. Andere geslachten waartoe de kikker in het verleden werd gerekend zijn Bufo (tegenwoordig: padden (Bufonidae) en het tegenwoordig niet meer erkende Bombinator. De synoniemen zijn hieronder weergegeven.
De vuurbuikpadden uit het geslacht Bombina worden soms ook wel tot de schijftongkikkers (Discoglossidae) gerekend.
De geelbuikvuurpad (Bombina variegata) is een padachtige kikker uit de familie Bombinatoridae en het geslacht vuurbuikpadden.
De kikker heeft een groot verspreidingsgebied in het midden en zuiden van Europa en komt onder andere voor in België en Nederland. Hier is de soort echter zeer zeldzaam en ernstig bedreigd.
Kumak górski (Bombina variegata) – gatunek płaza bezogonowego z rodziny kumakowatych (dawniej zaliczany do ropuszkowatych), blisko spokrewniony z kumakiem nizinnym. Cechuje się brązową grzbietową stroną ciała i kontrastującą z nią stroną brzuszną, pokrytą ostrzegawczym deseniem żółci i czerni. Występuje w Europie. Zasiedla różnorodne środowiska. Rozmnaża się w małych, często istniejących krótkotrwale zbiornikach wodnych, niekiedy zanieczyszczonych.
Kumaki zaliczano niegdyś do gromadzącej prymitywne płazy[3] rodziny ropuszkowatych[4][3]. Obecnie umieszcza się je w osobnej rodzinie kumakowatych[2], chociaż niektóre publikacje podają jeszcze starą systematykę[5].
Dawniej wyróżniano 4 podgatunki kumaka górskiego[6][3]:
Jednakże B. variegata pachypus została podniesiona do rangi odrębnego gatunku Bombina pachypus. Dokonali tego Lanza i Vanni w 1991, opierając się na danych elektroforetycznych, jak i morfologicznych. Jednakże wielu specjalistów wyraża odmienne zdanie (Ohler 1997, Bologna et al. 2000, Hofman et al. 2007)[7].
Przebadano między innymi mitochondrialny DNA kumaków. Badania te dostarczyły informacji o pochodzeniu gatunku i głównych liniach. Poziom różnorodności genetycznej wewnątrzgatunkowej kumaków nizinnego i górskiego były dla większości zbadanych loci podobne. Kumak górski cechował się większą różnorodnością w przypadku genu oksydazy cytochromowej i znaczne różnice pomiędzy haplotypami, które u kumaka nizinnego są sobie znacznie bliższe. Linia karpacka i alpejska różnią się od siebie w mtDNA statystycznie w 4,7–5,2%, ale poszczególne geny wykazują większe różnice. W przypadku wspomnianej oksydazy cytochromowej w sekwencjonowanym regionie wyniosły 8%, a w dehydrogenazie dinukleotydu nikotynoamidoadeninowego aż 10%[5].
Kumak górski i kumak nizinny są ze sobą blisko spokrewnione. Ich dalszym krewnym jest kumak dalekowschodni[5].
Próby wyjaśnienia zasięgów występowania europejskich kumaków pociągnęły za sobą powstanie kilku hipotez. Jedna z nich uznaje, że kumak nizinny i kumak górski powstały na skutek zmian klimatu związanych z jednym z plejstoceńskich zlodowaceń. Przeczy temu zapis kopalny, rozróżniający odrębne linie tych kumaków już od pliocenu. Zlodowacenia plejstoceńskie kumak górski prawdopodobnie przetrwał na Bałkanach i Półwyspie Apenińskim i wtedy powstały główne linie mtDNA, różniące się między sobą w 4,7–5,2%. Inne obszary Europy opanowały w czasie interglacjałów. Na Węgry zwierzę dostało się znad zachodniego Dunaju (Kraj Zadunajski). Populacje północne mogły przemierzyć dwie alternatywne drogi: przedostać się przez Karpaty lub drogą zachodnią znad Dunaju. Obecnie wyróżnia się dwie główne linie gatunku: alpejską (zachodnią) i karpacką (wschodnią), do której zaliczają się też osobniki z północnego wschodu Węgier. Wydaje się, że klad karpacki wykazuje większą stabilność, być może przetrwał on też zlodowacenie w jakichś ostojach na terenie Europy Środkowej. Duże zróżnicowanie genetyczne wskazuje też na rozdrobnienie jego populacji już przed przybyciem na te tereny kumaka nizinnego. Natomiast w zachodniej części Węgier doszło do hybrydyzacji i zastąpienia kumaka górskiego nizinnym[5].
Kumak górski przypomina wyglądem kumaka nizinnego[4]. Nie zalicza się do dużych płazów: osiąga od 4[3] do 5[4][8][3]–5,5 cm długości[9].
Płaz ma spłaszczone ciało podtrzymywane przez rozstawione szeroko kończyny[3].
Źrenice cechują się kształtem sercowatym[9], trójkątnym[6] o wierzchołku skierowanym ku dołowi[3]. Bębenek nie występuje, podobnie jak rezonatory samców[6].
Kręgi odcinka krzyżowego kręgosłupa cechują się poszerzonymi wyrostkami poprzecznymi[6]. Długość piszczeli stanowi cechę rozróżniające środkowoeuropejskie kumaki[5].
Występuje dymorfizm płciowy w obrębie palców. Samce rozwijają na opuszkach specjalne zgrubienia. Występują one na pierwszych trzech palcach kończyn przednich[6] oraz na drugim, trzecim i czwartym palcu tylnych łap[3]. W okresie rozrodu towarzyszy im podobny twór na wewnętrznej powierzchni przedramienia[6]. Ma on ciemną barwę. Struktury takie noszą miano modzeli. Samca wyróżniają poza tym masywniejsze ramiona[3].
Niektóre z podanych wyżej cech odróżniają kumaka górskiego od nizinnego. Jednakże aby wiarygodnie zdiagnozować gatunek, należy ocenić całe zespoły, a nie pojedyncze cechy[6]. Dodatkowo w rejonach symapatrycznego występowania tworzą się mieszańce, tak więc diagnostyka na podstawie wyłącznie cech morfologicznych nie zawsze jest możliwa[5].
Zwierzę to wyróżnia się swym ubarwieniem. Wierzchnia strona jego ciała pełni rolę maskującą[3]. Jest brązowa[8], błotnista[3], ciemnooliwkowa[6], szarawa[3], gliniastoszara, ziarnista. Może też być odcieniu zielonkawego, a zdarza się, że i zielonego[4]. Zdobią ją ciemniejsze plamki. Natomiast białe punkciki są rzadkie albo też nie ma ich wcale[6]. Pokrywają ją brodawki[4], na szczycie zaopatrzone w pory i, zwłaszcza w przypadku płci męskiej, w kolce rogowe[3]. Guzki grzbietu są więc ostre i względnie wysokie[6], a skóra jest szorstka w dotyku[3]. W okresie rozrodu tworzą się tam zrogowaciałe narośla stożkowatego kształtu[4]. Ta strona ciała w odróżnieniu od spodniej nie jest tak łatwo dostrzegalna[3]. Podgatunek B. v. scabra charakteryzuje się bardziej kolczastymi brodawkami, niż u B. v. variegata[3].
Strona brzuszna zupełnie nie przypomina grzbietowej. Jest gładka w dotyku[3] i zabarwiona jaskrawożółto, pokryta plamami koloru niebieskoczarnego[8] lub też, wedle innej koncepcji opisu, czarną powierzchnię pokrywają żółte plamy. Dotyczy to brzucha, podgardla i brzusznej strony kończyn[9]. Obszary koloru żółtego obejmują delikatne czarne kropki. Na polach czarnych mogą co prawda występować białe punkty, jak u kumaka nizinnego, ale występują one co najwyżej skąpo albo nie ma ich w ogóle[3]. Istnieją też osobniki pomarańczowe[6], ubarwieniem przypominające kumaka nizinnego. Zamieszkują one tereny podgórskie[4]. Opisane umaszczenie sprawia wrażenie marmurkowania[3]. Guzki występują tutaj rzadko rozmieszczone, osiągają też małe rozmiary[4]. Spodnia strona kończyn odpowiada ubarwieniem brzuchowi. Końce palców są jasne[6], koloru żółci lub pomarańczu, jak brzuch zwierzęcia. Odróżnia to B. variegata od B. bombina o palcach ciemnych lub jaśniejszych, ale nie jaskrawych. Kolejna żółta plama może znajdować się u omawianego płaza na tylnej stronie uda. Podgatunek bałkański B. v. scabra wyróżnia się bardziej żółtym brzuchem, niż u podgatunku nominotypowego. Jeszcze mniej czarnych plam pokrywa brzuch podgatunku z Dalmacji: B. variegata kolombatovici[3].
Gruczoły skórne B. variegata produkują żrącą wydzielinę. Drażni ona błony śluzowe zainteresowanego zjedzeniem kumaka mięsożercy, ma także działanie wymiotne. Może ona także uczulać[3]. W skórze kumaka górskiego znaleziono peptydy o właściwościach antybakteryjnych. Pierwszym z wyizolowanych peptydów przeciwdrobnoustrojowych, odkrytych na początku lat sześćdziesiątych XX wieku, była bombinina. Odkryto też kolejne. Składają się one z 27 reszt aminoacylowych, przy czym reszty aminokwasowe od 14 do 27 nie różnią się od siebie. Zmienność dotyczy więc fragmentu N-końcowego. Przypominają one bombininę, chociaż nie są z nią identyczne. Działają one w największym stopniu na pałeczkę okrężnicy i gronkowce[10].
Tryb życia kumaka górskiego przypomina ten obserwowany u kumaka nizinnego[9].
Jest to zwierzę ciepłolubne[9]. W Europie Środkowej spotyka się je od kwietnia do września[8]. Z końcem września –
początkiem października płaz ten udaje się na spoczynek zimowy. Znajduje jamę czy miejsce pod kamieniami lub kłodami drewna, gdzie zapada w stan hibernacji. Okres powrotu do aktywności zależy od podwyższenia się temperatury, przypada więc na czas od marca do maja[6] (wedle innych źródeł jest to marzec – kwiecień[3]). Jeśli żyje w źródłach hydrotermalnych, płaz w ogóle nie musi zapadać w sen zimowy[6].
Może być aktywny w ciągu dnia, spędza go bowiem w wodzie, która chroni go przed wysychaniem[8]. Aktywnie spędza dzień w leśnych kałużach czy zacienionych, zalanych wodą żwirowniach. Najczęściej za dnia przebywa jednak ukryty. Gdy siedzi zanurzony w błocie, nad powierzchnię wystawia tylko oczy. W wodzie rozpościera kończyny ukośnie na boki. Często wypoczywa w płytkiej wodzie. Uaktywnia się wieczorem[3]. Niektóre samice pozostają w zbiornikach wodnych już po skończeniu okresu rozrodczego, aż do jesieni[11].
Kumak pływa za pomocą krótkich, odbijających ruchów nóg. Nierzadko nurkuje. Gdy coś go zaniepokoi, ukrywa się pośród mułu[3].
Jako że wykorzystuje do rozrodu nietrwałe, niewielkie zbiorniki wodne, podatne na zmiany, jego sukces rozrodczy zależy silnie od możliwości przemieszczania się, a także znajomości terenu. Badania tej kwestii przeprowadzono w Rumunii w latach 2003–2005. Nieliczne osobniki odłowiono kilkakrotnie w różnych stawach (prawdopodobnie z powodu lądowego trybu życia tych zwierząt). Na tej podstawie obliczono średnią odległość między stawami, w których kumaki górskie dokonywały rozrodu, wynosiła 161 m dla samców, 172 m dla samic, przekraczając medianę równą w obu przypadkach 122 m. Największa zanotowana odległość pomiędzy takimi stawami pochodzi ze Szwajcarii, z terenów otwartych, wynosząc 240 m. Nie wykazano tutaj istotnych różnic w zależności od płci. Zupełnie inaczej natomiast przedstawiała się zależność pomiędzy rozmiarami zwierzęcia (mierzoną od czubka pyska do ujścia kloaki) i przemierzanymi przezeń odległościami. U samców statystycznie istotna zależność nie istniała. U samic znaleziono taką zależność, co więcej, różnice w zmierzonym wymiarze ciała odpowiadały za 40% różnic w przemierzanej przez płazy odległości. Być może większe, a więc i starsze samice lepiej radziły sobie ze znajdywaniem nowych zbiorników wodnych. Przywołuje się tu także ogólną dla płazów zależność, zgodnie z którą im większa samica, tym więcej jaj wytwarza. Dlatego większe samice, osiągając nowe zbiorniki wodne, zmniejszają przez to konkurencję, na którą narażają swe potomstwo. Dodatkowo im większa odległość pomiędzy zbiornikami wodnymi, tym rzadsze są migracje pomiędzy nimi. Z 75 stawów obecnych na terenie zajmowanym przez populację z Rumunii, 65 było objętych migracją, a w 21 odnotowano rozród (nie wszystkie były dlań odpowiednie w bardziej suchych sezonach). Mniejsze, niezdatne do rozrodu zbiorniki mogą też służyć jako przystanki podczas podróży. Kumaki wcześniej spotkane w stawie odławiano też na lądzie, w odległości nie przekraczającej 1300 m. Wcześniejsze badania Gollmana i współpracowników wykazały, że w austriackim lesie mieszanym poprzecinanych terenami trawiastymi samce przemierzały pomiędzy odłowami od 90 do maksimum 980 m, podczas gdy samice 150 m, maksymalnie 600 m. W Starej Płaninie w Bułgarii płazy te przebywały mniejsze dystanse: 64 m w przypadku samców i 20 m u płci przeciwnej. Fakt, że nie złapano w cytowanym badaniu rumuńskim osobników młodych z poprzedniego sezonu przemawia za emigracją tych osobników. Największe dystanse przebywają one podczas pierwszych 2–3 lat życia po przyjęciu postaci dorosłych płazów, o czym pisali w 2000 Gollmannowie, według których bezogonowy nabywa także w ten sposób wiedzy odnośnie otaczającego go środowiska. Nie muszą one jednak wtedy zaglądać do miejsc rozrodu. Być może niektóre z nich wracają do miejsc, w których przyszły na świat, gdy dojrzeją do wydania nowego pokolenia. Z drugiej strony nowo utworzone po opadach zbiorniki zdatne do rozrodu były przez B. variegata szybko zajmowane. Nie można jednak wykluczyć, że młodych kumaków górskich nie łapano z uwagi na znaczną umieralność, ale ten okres życia wiąże się z największych rozpraszaniem się zwierząt także u innych płazów, takich jak kumak nizinny czy ropucha paskówka[12].
Przebywane przez kumaki dystanse mogą też zależeć od pory roku. Latem w Niemczech odnotowano pokonywanie dystansu 20–30 m. Natomiast w drodze do swych zimowych siedlisk zwierzęta przebywały do 650 m. Rolę mogą tu odgrywać także warunki pogodowe. Samice przebywają większe dystanse wraz ze wzrostem opadów. Być może testują dzięki temu większą ilość zbiorników pod kątem przydatności do rozrodu, a podczas deszczowej pogody więcej miejsc się do tego nadaje. Samice mogą nawet konkurować o to, które wcześniej zajmą nowe miejsca rozrodu. Podobnej zależności nie wykazano u samców[12].
Natomiast w innym badaniu, przeprowadzonym w okolicach Zurychu, 75% samców i 85% samic zawsze znajdywano w tym samym lub w jednym z przyległych stawów, co wskazuje jednak na przywiązanie kumaka do miejsca[11].
Zaniepokojony na lądzie, kumak górski przybiera pozycje ostrzegawczą[8], czyli tak zwany odruch czy też refleks kumaka[3]. Wygina wtedy grzbiet i odwraca się[9], wyginając ku górze kończyny. Z załamanym ku tyłowi grzbietem[3] pokazuje jaskrawo ubarwiony spód ciała[8], której czarno-żółty wzór ma za zadanie ostrzegać drapieżnika przez spożyciem niejadalnego płaza, pokrytego żrącą, drażniącą i wymiotną wydzieliną gruczołów skóry[3].
Głos tego płaza określa się jako u[3] lub uuh-uuh-uuh. Jest on cichy, lecz melodyjny. Różni się od kumkania kumaka nizinnego częstością drugiej zapisanej frazy, przekraczającą 40/min[9]. U ma się powtarzać dwukrotnie na sekundę. B. variegata kumka więc szybciej i dźwięczniej[3], ciszej i zarazem wyżej[6]. Człowiekowi trudno jest stwierdzić, skąd dochodzi taki głos[3].
Cykle życiowe obu środkowoeuropejskich gatunków kumaków nie przedstawiają większych odrębności[4].
Kumak górski rozmnaża się w środowisku wodnym. Wykorzystuje do tego celu nawet najmniejsze zbiorniki wodne[8], często nietrwałe[2]. Ważne, by były ciepłe i płytkie[9], niezacienione, zwłaszcza leżące w lesie lub jego pobliżu[2]. Mogą to być sadzawki o wspomnianych cechach, ale korzysta także z zalanych wodą dawnych wyrobisk żwiru, większych kałuży, a nawet gromadzących wodę kolein[9]. Różni się tym od kumaka nizinnego, preferującego większe, bardziej trwałe zbiorniki[13]. Ważną cechą jest brak innych płazów, a właściwie ich larw. Szczególnie unika żaby trawnej i żaby dalmatyńskiej. Larwy te mogłyby stanowić zagrożenie jako drapieżniki. Udowodniono choćby żywienie się kijanek żaby dalmatyńskiej jajami kumaka górskiego. W takich warunkach znacznie zwiększa się umieralność larw B. variegata. Również obecność kijanek własnego gatunku czyni zbiornik mniej atrakcyjnym[12].
Okres rozrodczy rozpoczyna się 5–10 dni po wkroczeniu do wody[6]. Samce gromadzą się razem, choć usadawiają się w pewnej odległości od siebie, od 35 do 50 cm. Tworzą w ten sposób rewiry[3]. Samce konkurują między sobą, ponieważ ilość samców i samic nie jest identyczna – niekiedy na jedną samicę w obszarze rozrodczym przypada 5 samców (w lesie proporcje są bardziej wyrównane)[11]. Jeśli jakiś samiec wtargnie na teren zajęty już przez innego, jego właściciel odpycha go tylnymi kończynami[3]. Samiec nie posiada worków rezonansowych[3][6], nawołuje jednak samice[9]. Tworzy się w ten sposób kumkający chór. Samce nie ograniczają się jednak do wydawania odgłosów – uderzają nogami w dość regularnym tempie. W ten sposób powstają fale rozchodzące się po powierzchni wody. Zarówno dźwięki, jak i fale stanowią sygnały dla płci przeciwnej. Koncerty odbywają się przeważnie wieczorami i wczesną nocą, niekiedy za dnia. Jeśli temperatury są niskie, zwierzęta mogą kontynuować to zachowanie aż do lata[3]. Wedle Kuzmina rozród trwa aż do sierpnia[6].
Rozród może przebiegać wielokrotnie w czasie tego samego sezonu. Często następuje po ulewnych deszczach, które napełniają tymczasowe zbiorniki wodne[12][11]. Brak odpowiednich warunków z powodu suszy nie powoduje nadrobienia tego przy ich zmianie. Liczba nocy, podczas których odbywa się składanie skrzeku, różni się w zależności od roku, w przeciwieństwie do ilości składanych podczas nocy jaj ani ilości wykorzystywanych do tego zbiorników wodnych[11].
Samica, która jest gotowa do rozrodu, odwiedza rewir zajęty przez samca. Zachodzi ampleksus pachwinowy[3], miedniczy[6]. Polega on na tym, że samiec, wykorzystując opisane wyżej modzele godowe na przedramionach i opuszkach palców, chwyta swą wybrankę w pachwinach[3]. Nie występuje rozdział czasowy pomiędzy ampleksusami a składaniem skrzeku i dojrzewaniem kijanek innych osobników. Niekiedy intensywne składanie skrzeku w niewielkich zbiornikach wodnych następuje po intensywnych letnich deszczach. Jaja tworzą składane porcjami kłęby, liczące od 45 do 100, a nawet więcej jaj[6]. Najmniejszy z kłębów zbieranych w okolicy Zurychu liczył 4 jaja, największy – 960. Średnia wyniosła 84[11]. Matka może również składać je pojedynczo. Umieszcza je na wodnych roślinach, kamieniach, gałęziach, a samiec dokonuje zapłodnienia (zapłodnienie zewnętrzne). Samica może wielokrotnie w tym samym sezonie rozrodczym przystępować do rozmnażania. Tymczasem po złożeniu jaj mija 8 dni, po których wylęgają się larwy zwane kijankami. Dorastają one długości 3–5 cm, nim pod koniec lata przystąpią do przeobrażenia. Nie wszystkie zdążą przejść metamorfozę w pierwszym roku swego życia, niektóre będą zimować w postaci larwalnej. Jednakże brak jednego terminu rozrodu wiąże się z większymi szansami na sukces rozrodczy, zwłaszcza w przypadku płaza wykorzystującego do tego celu efemeryczne zbiorniki wodne, które mogą w niedługim czasie wyschnąć, zabijając potomstwo. Zmniejsza to również konkurencję wśród larw, gdyż zasoby pożywienia w małych zbiornikach nie należą do obfitych[3].
Duże zagęszczenie kijanek zwiększa ich umieralność. W przypadku współwystępowania kijanek w różnym wieku negatywny efekt dotyczy głównie tych starszych[12].
Osobniki młodociane wynurzają się ze zbiorników wodnych między czerwcem a sierpniem. Przed zimowaniem mierzą one od poniżej 15 do 28 mm[11].
Nie wszystkie kumaki górskie osiągają dojrzałość płciową w tym samym czasie. Niektóre już latem, gdy mają około roku, osiągają rozmiary dorosłych płazów. Barandun i współpracownicy wątpią jednak, by przystępowały one do rozrodu. Dojrzałość płciowa zazwyczaj następuje po przeżyciu 2–3 zim, a w niektórych przypadkach jeszcze później[11].
W 1992 oznakowano prawie całą populację i znaleziono tylko nieliczne młode osobniki dorosłe. W innym badaniu 45% złapanych w 1993 osobników zidentyfikowano jako płazy, które odłowiono poprzednio w 1990. Wynika z tego, że chodzi o zwierzęta w wieku minimum czterech lat. W 1991 i 1992 obliczono roczną przeżywalność dorosłych osobników na 58% u samic i 63% u samców (średnio 62%). Jednakże migracje czy kwestie odłowu podważają wiarygodność tego wyniku – w rzeczywistości przeżywalność musi być większa. Brak spadku liczby osobników w bardziej zaawansowanym wieku wskazuje na wysoką przeżywalność. Natomiast różnice pomiędzy płciami w tym względzie wyjaśniają przewagę ilości samców w populacji[11].
Pomimo różnych preferencji środowiskowych[13] w rejonach, gdzie spotykają się oba gatunki, odnotowano regularne krzyżowanie się kumaka górskiego z nizinnym[2].
Przykładem takiej okolicy są słowacko-węgierskie obszary krasowe. Gollmann i współpracownicy opisują za Láciem panującą tam szczególną sytuację: kumak górski zamieszkuje dolinę rzeki Slany, podczas gdy kumak nizinny bytuje na wyżej położonych obszarach Silickiej planiny, gdzie panuje cieplejszy klimat, ale też bardziej zaznacza się działalność ludzka. W kilku miejscach napotkano osobniki heterozygotyczne dla wszystkich badanych loci przy nieobecności osobników należących do rozpatrywanych gatunków. Wskazuje to, że mieszańce nie pochodziły bezpośrednio od nich, ale od innych mieszańców. W innych miejscach przeważają osobniki różnego typu przy współwystępowaniu innych. Osobniki czyste gatunkowo zamieszkują centrum omawianego obszaru. Autorzy zwracają też uwagę częste występowanie tam allelu Ldh-lM, co może stanowić efekt dryfu genetycznego, odmiennej presji selekcyjnej na tym obszarze lub błędu przy pobieraniu próbek[13].
Wąska strefa hybrydyzacji wydaje się stabilna. Zjawisko takie tłumaczy się różnymi hipotezami (mniejszym dostosowaniem mieszańców, większym dostosowaniem hybryd do specyficznych warunków w strefie hybrydyzacji, doborem faworyzującym inne allele po obu stronach strefy krzyżowania się). Z uwagi na różnice gatunkowe ostatnia z wymienionych propozycji wydaje się odgrywać największą rolę, choć z drugiej strony zwiększona umieralność zarodków w centrum strefy hybrydyzacji wskazuje na selekcję wymierzoną przeciwko mieszańcom[13].
W Rumunii również istnieje strefa hybrydyzacji zupełnie pozbawiona osobników należących do gatunków rodzicielskich. Strefy hybrydyzcji odnaleziono również w Polsce i w Chorwacji. W tych państwach strefy te są wąskie. Liczą od 6 do 9 km szerokości, jeśli krańce zdefiniuje się poprzez obecność czystych genetycznie przedstawicieli gatunków[5].
Kumak górski należy do płazów europejskich. Zajmuje większą część Europy Środkowej i Południowej[2], żyje też w Europie Zachodniej[9]. Na zachodzie zasięg jego występowania sięga środkowej Francji, a nawet północnego zachodu tego kraju, gdzie problem stanowi jednak znaczna fragmentacja. W Luksemburgu, jak i w Holandii istnieje po jednej samotnej populacji. Główna część zasięgu przebiega przez środkowe Niemcy (Dolna Saksonia, Turyngia[9]), podczas gdy na północy tego kraju spotyka się izolowane populacje. Obejmuje Karpaty, północ i zachód Szwajcarii i północno-wschodnie Włochy. Izolowane populacje zamieszkują również na Węgrzech. Zasięg zmierza dalej na Bałkany[2].
Lista państw, gdzie występuje, przedstawia się wedle IUCN następująco: Albania, Austria, Bośnia i Hercegowina, Bułgaria, Chorwacja, Czarnogóra, Czechy, Francja, Grecja, Holandia, Liechtenstein, Luksemburg, Macedonia Północna, Niemcy, Polska, Rumunia, Serbia, Słowacja, Słowenia, Szwajcaria, Ukraina, Węgry, Włochy[2]. Inne źródła podają także Belgię, Mołdawię, nie wymieniają zaś Bośni i Hercegowiny[6].
Główna część powyżej opisanego zasięgu odpowiada podgatunkowi Bombina variegata variegata[6]. Spotyka się go we Francji, Beneluksie z pominięciem terenów blisko wybrzeży, na zachodzie i południu Niemiec, w Polsce, Czechach, na Słowacji, w Aplach i na Bałkanach[3]. Inny podgatunek, B. variegata kolombatovici, zamieszkuje tereny byłej Jugosławii: Dalmację i Czarnogórę[6] (niekiedy wymienia się tylko Dalmację[3]). B. variegata pachypus spotyka się we Włoszech[6], na południe od Padu[3]. B. variegata scabra żyje w Grecji, Albanii, Czarnogórze i Bułgarii[6].
W Polsce spotyka się go prawie wyłącznie w Karpatach[8]. Marian Młynarski podaje, że pospolity jest w Karpatach i na pogórzu tego pasma górskiego, a wyspowo występuje także na grzbiecie Wyżyny Krakowsko-Częstochowskiej[4]. Żyje tu podgatunek nominatywny. Wedle niektórych źródeł spotkać go można także na wschodnim przedgórzu Sudetów i Grzbiecie Krakowsko-Chrzanowskim[3].
W Belgii prawdopodobnie płaz wymarł. Taki sam los mógł spotkać populacje zamieszkujące w przeszłości południową Francję. Istnienie izolowanych populacji w Médoc czy Landy wymaga potwierdzenia[2]. W obrębie Basenu Karpackiego płaz występuje wyspowo na terenach górzystych. Jego populacje są w nim otoczone populacjami kumaka nizinnego[5].
Podjęto próbę introdukcji zwierzęcia w Wielkiej Brytanii. Jej efekty dla chwili obecnej nie zostały jeszcze poznane. Państwa tego zazwyczaj nie wymienia się jeszcze, opisując zasięg występowania kumaka górskiego[2].
Region sympatrycznego występowania kumaka nizinnego obejmuje Polskę, Słowację, Węgry, Austrię, Rumunię, Bułgarię i Chorwację[5].
Płaz zasiedla głównie góry i pogórza[8], a także wyżyny[4]. Zamieszkuje wysokości od 100 do 2100 m nad poziomem morza[2] (niektóre źródła podają do 1900 m n.p.m.[9] czy 1500–2000 m n.p.m.[3]). W Tatrach jego górną granicę zasięgu wyznacza wysokość 1600 m n.p.m.[4][3]
Bombina variegata zasiedla różnorodne siedliska. Należą do nich lasy, zarówno iglaste (zamieszkuje je na większych wysokościach nad poziomem morza, tak jak leśne polany), jak liściaste (w tych żyje zwłaszcza na niższych wysokościach) i mieszane, busz, łąki i inne tereny trawiaste, równiny zalewowe[2]. Wykazuje mniejszą, niż swój nizinny krewniak, zależność od środowiska wodnego. W okresie słoty urządza wędrówki w poszukiwaniu nowych zbiorników[4].
Płaz zajmuje różnorodne zbiorniki wodne takie jak stawy, jeziora, rzeki, bagna, strumienie (niekiedy o wartkim nurcie[6], choć raczej unika wód płynących[3]) i tworzone przez nie zbiorniki wodne, źródła, w tym także źródła wód mineralnych i termalnych, kałuże[2].
Jako siedliska zajmuje często środowiska wytworzone przez człowieka[9]. Zamieszkuje w rezerwuarach wody, rowach[2], kamieniołomach, piaskowniach, żwirowniach czy gliniankach, w obrębie których znaleźć może płytkie zbiorniki wodne, słabo zarośnięte[2] (nie licząc rzęsy[3]), o niewielkiej powierzchni[9]. Spotykano go nawet w gnojówkach przy gospodarstwach rolniczych[4], a także na torfowiskach wysokich i w dołach potorfowych, cechujących się niskimi pH[3], oraz w wodach silnie zanieczyszczonych, bogatych w sole i kwas siarkowodorowy. Zamieszkuje też parki śródmiejskie[6].
Kumak górski najczęściej zasiedla zbiorniki wodne, w których nie spotka innych płazów. Wyjątkowo dzieli je z kumakiem nizinnym[3].
Pożywieniem kumaka górskiego są głównie stawonogi lądowe, co wiąże się z jego bardziej lądowym trybem życia, niż w przypadku kumaka nizinnego. Na brzegach strumieni jego ofiarą padają także bezkręgowce wodne, zwłaszcza Gammaridae[6]. Inne źródło podaje skąposzczety, jak też inne zwierzęta niedużych rozmiarów[3]. Ułamek organizmów wodnych w diecie płaza nie zmienia się z jego wiekiem, w przeciwieństwie do wielkości zdobyczy: starsze kumaki górskie częściej polują na większą zdobycz[6].
W 2004 Międzynarodowa Unia Ochrony Przyrody przyznało kumakowi górskiemu status gatunku najmniejszej troski (LC – Least Concern). Istnieje wiele miejsc, gdzie ciągle występuje on pospolicie. Należą do nich Karpaty, w tym Polska, Słowenia. W lasach karpackich osiąga niekiedy znaczne zagęszczenie[2] wynoszące w wielu dogodnych miejscach jednego kumaka na kilka m², dochodzące do jednego osobnika na 0,02 m². Kumak górski uchodzi nawet za najpospolitszego płaza zasiedlającego szeroką gamę środowisk[6].
Zachód i północny zachód zasięgu występowania cechuje się dużą fragmentacją populacji. Miały tam również miejsca lokalne wyginięcia, jak też spadki liczebności. Wśród miejsc takich wymienia się południową Szwajcarię, Niemcy, północno-zachodnią i południową Francję[2]. Zła jest sytuacja na Ukrainie, w obwodzie lwowskim i zakarpackim. W ciągu dwóch minionych dekad miała tam miejsce presja ze strony działalności ludzkiej, która doprowadziła do wyginięcia bezogonowego w 13 lokalizacjach[6].
Pomimo że w skali globalnej gatunek nie jest poważnie zagrożony, niestety całkowita liczebność obniża się. Istnieją różne zagrożenia lokalne. Należą do nich degradacja środowiska naturalnego spowodowana działalnością człowieka, urbanizacja, budowa dróg, przemysł, zwłaszcza związany z wydobyciem i transportem ropy, zanieczyszczenie zbiorników wodnych, choć płaz ten toleruje zanieczyszczenie wody[2], według Młynarskiego nawet silne[4]. Bytuje w nich pomimo znacznego zasolenia i obecności kwasu siarkowodorowego[6]. Poza tym niekiedy rybacy wykorzystują go w roli przynęty. Odławia się go także i sprzedaje, by uczynić zeń zwierzę domowe lub laboratoryjne. Z drugiej strony zwierzęciu zagraża sukcesja ekologiczna terenów uprzednio zmodyfikowanych przez człowieka, na których kumak czuje się dobrze. Przeszkadza mu bowiem zarastanie zbiorników po żwirowniach i gliniankach[2], niekiedy też zbiornikom tym zagraża drenaż[12]. Niekorzystny efekt odgrywa również hybrydyzacja ze swoim krewniakiem Bombina bombina. W Transylwanii hybrydyzacja mozaikowa doprowadziła do utraty czystych genetycznie populacji[2].
Gatunek wymienia załącznik II Konwencji o ochronie gatunków dzikiej flory i fauny europejskiej oraz ich siedlisk (konwencji berneńskiej), jak też załącznik IV dyrektywy siedliskowej (wcześniej II[12]). Podlega także ochronie prawnej w krajach obejmujących większą część jego zasięgu[2], m.in. w Polsce[3]. Jego zasięg występowania obejmuje także wiele obszarów chronionych[2].
Z drugiej strony IUCN zauważa jednak potrzebę ochrony jego siedlisk, zwłaszcza terenów podmokłych. Proponuje nawet ograniczanie sukcesji zarośli i lasów w takich miejscach[2]. Ważną rolę odgrywa również odpowiednie zagęszczenie zbiorników wodnych w rejonach rozrodu[12]. IUCN zauważa też konieczność monitoringu gatunku w pewnych obszarach, wśród których wyróżnia szczególnie miejsca współwystępowania obu kumaków: górskiego i nizinnego, na których zachodzi krzyżowanie się. Stwierdza także możliwość potrzeby reintrodukcji[2].
Kumak górski (Bombina variegata) – gatunek płaza bezogonowego z rodziny kumakowatych (dawniej zaliczany do ropuszkowatych), blisko spokrewniony z kumakiem nizinnym. Cechuje się brązową grzbietową stroną ciała i kontrastującą z nią stroną brzuszną, pokrytą ostrzegawczym deseniem żółci i czerni. Występuje w Europie. Zasiedla różnorodne środowiska. Rozmnaża się w małych, często istniejących krótkotrwale zbiornikach wodnych, niekiedy zanieczyszczonych.
Bombina variegata é uma espécie de anfíbio anuro pertencente à família Bombinatoridae e ao género dos sapos-de-barriga-de-fogo.
Adulto: Os machos e fêmeas maiores medem entre 35 e 55 mm, sendo por isso bastante pequenos para Archaeobatrachia. A sua parte superior é cinzento-acastanhado, muitas vezes com manchas claras e esbatidas. A sua barriga, incluindo a parte de dentro dos membros e dedos é cinzento-azulado a preto-azulado com pintas ou manchas amarelas até alaranjadas brilhantes, normalmente cobrindo mais de metada da barriga. Estes sapos têm um corpo compacto, embora não tão achatado com as suas parentes próximas Bombina bombina, e um focinho arredondado. As pupilas são em forma de coração e os tímpanos não são visíveis. A face tem muitas verrugas.
A chamamento dos machos pode ser ouvido na fim da Primavera e princípio do Verão, com um fraco mas melódico "uh… uh… uh" a partir dos locais de reprodução. Como esta espécie não tem saco vocal, em contraste com Bombina bombina, o seu chamamento é bastante suave.
Bombina variegata é uma espécie de anfíbio anuro pertencente à família Bombinatoridae e ao género dos sapos-de-barriga-de-fogo.
Kunka žltobruchá (iné názvy: kunka vrchovská, zastarano: kunec žltobruchý, kunec žltkavý, kunec žltkastý [1]; lat. Bombina variegata) je druh žaby. Ide o menšiu žabku, ktorá je výrazným obyvateľom malých vodných nádrží.
Táto žabka dosahuje veľkosti 5,5 cm[2]. Zvrchu má hnedastú až sivozelenú farbu. Na dotyk drsná, pretože má ostro zakončené kožné bradavky. Hlavu má plochú, širokú a okrúhlu. Viac ako 50 % plochy brucha má výrazne žltú farbu s veľkými sivými až čiernymi škvrnami. Samec vlastní tmavé rohovité plochy na predlaktí a prstoch. Tie využíva predovšetkým v čase párenia. Hlas tohto obojživelníka znie veľmi príjemne. Ide o pomerne tiché „ung“ alebo „uh“. Kunka má zaujímavo vyzerajúcu zrenicu oka v tvare srdca.
Typickým miestom výskytu a rozmnožovania sú malé dočasné vodné plochy. Môže ísť aj o vyjazdené koľaje na nespevnených lesných cestách. Vo väčšej obľube má radšej vyššie polohy – od 250 do viac než 1 200 m n. m. Pri kladení svojich vajíčok uprednostňuje slnečné nezatienené miesta. Táto žabka je aktívna cez deň aj v noci. Počas dňa často leží vo vode alebo odpočíva na plytčine pri brehu. Pláva krátkym tempom. Veľmi často sa potápa. Ak je vyrušená, ukryje sa v bahne. Práve tu jej slúži jej vrchné sfarbenie ako maskovanie. V prípade nebezpečenstva na súši zaujme výstražný postoj (zdvihne predné a zadné nohy, prehne chrbát) a odhalí odstrašujúce sfarbenie brucha. Ide o varovný signál, ktorý upozorňuje, že je tento živočích je nejedlý. Vylučované kožné sekréty sú žieravé a môžu spôsobiť alergickú reakciu. Dráždi ústnu sliznicu a pôsobí odporne.
Zimu prečkáva v bahne vo vode alebo na súši zahrabaná v zemi.[3]
Ide výhradne o európsky druh. Vyskytuje sa na západ od Francúzska až po karpatský masív a od stredného Nemecka a južného Poľska, ďalej Taliansko a Balkán.
Jej populácia je široko roztrúsená v sekundárnych biotopoch – napr. kameňolomy, pieskovne, štrkovne a ťažiská ílu, ktoré sú zaplavené plytkou, príliš nezarastenou vodou. Na Morave je jej populácie výrazne rozšírenejšia a menej ohrozené ako v Čechách.
Kunka žltobruchá je polytypický druh so 4 poddruhmi. Na území Slovenska sa vyskytuje nominotypický poddruh.[4]
Táto kunka dokáže zniesť aj silné organické znečistenie vody. Hlavnou príčinou miznutia celých populácií je devastácia prostredia – veľkoplošná aplikácie biocídov, miznutie a intoxikácie vhodných stanovíšť. V lesoch je na vine používanie ťažkej mechanizácie a povrchové úpravy ciest asfaltovaním. Ďalším faktorom je zriaďovanie skládok v mieste bývalých lomov. Niektorými rybármi je používaná ako návnada a zriedkavo sa hromadne zbiera na zberateľské a vedecké účely.
Je chránená bernským dohovorom a patrí do sústavy Natura 2000[2]. V Česku ide o silne ohrozený druh podľa vyhlášky č. 395/1992 Zb.
Na jar začínajú samce vydávať svoje charakteristické volanie[2]. Pritom si udržujú vzájomný, asi 50 cm odstup. V prípade priblíženia iného samčeka sa ho „majiteľ územia“ pokúša odstrčiť zadnými nohami. Podľa zborového volania samčekov samičky ľahko nájdu miesto rozmnožovania. Samičku pripravenú k rozmnožovaniu samček pomocou hrbolčekov na prstoch a predlaktiach pevne objíme v oblasti bedier (tzv. amplexus inguinalis). Samček potom oplodní asi 150 vajíčok, ktoré samička kladie jednotlivo alebo v malých zhlukoch na vodné rastlinstvo, kúsky konárov alebo kamene. Samičky sa môžu počas leta rozmnožovať aj niekoľkokrát. Nádej vajíčok a žubrienok na prežitie, v malých nestálych vodných nádržiach, sa tak veľmi zvyšuje. Žubrienky sa liahnu približne po dvoch týždňoch. Po dvoch mesiacoch sa premenia na malé žabky. V druhom až treťom roku života dochádza k pohlavnej dospelosti.
Môže dochádzať ku kríženiu s kunkou červenobruchou.[4][5]
Živí sa červami, larvami komárov a inými drobnými živočíchmi.
Kunka žltobruchá (iné názvy: kunka vrchovská, zastarano: kunec žltobruchý, kunec žltkavý, kunec žltkastý ; lat. Bombina variegata) je druh žaby. Ide o menšiu žabku, ktorá je výrazným obyvateľom malých vodných nádrží.
Hribski urh (znanstveno ime Bombina variegata) spada v družino žab urhov Bombinatoridae. Vpisan je na seznam ogroženih živalskih vrst v Sloveniji.
Hribski urh zraste v dolžino med 35 in 55 mm. Po zgornji strani telesa so sivo rjave barve s svetlimi pikami in bradavicami. Po trebuhu so sivo modre ali črno modre barve, posejane s svetlo rumenimi ali oranžnimi pikami ali lisami. Zenice imajo obliko srca, v ušesih pa ni videti bobniča.
Parjenje poteka pozno spomladi ali v začetku poletja, ko se samci oglašajo z značilnim melodičnim "uh... uh... uh".
Mrest sestavlja od 2 do 30 jajčec, ki so pritrjena na travo ali drugo rastlinje. Jajčeca so po zgornji strani rjave, po spodnji pa svetle barve in merijo v premeru od 1,5 do 2 mm. Sluz, ki jih ovija, je debela od 5 do 8 mm. Jajčeca samice odlagajo konec maja in v juniju.
Paglavci so v zadnjem stadiju razvoja dolgi okoli 55 mm, konica repa pa je pri paglavcu hribskega urha zaobljena. Barva paglavcev je umazano siva in se mavrično preliva.
Hribski urh se zadržuje v neposredni bližini voda, običajno ob potokih in rekah. Pogosto se zadržuje tudi v mlakah gozdnih poti v bližini stalnih vodnih virov. V take mlake najraje odlaga jajčeca, saj se zaradi višjih temperatur vode v njih paglavci hitreje izvalijo. Hribski urh je sposoben prepotovati večje razdalje, zaradi česar se uspešno širi izven svojega okolja. Zadržuje se v višje ležečih delih Evrope.
Hribski urh (znanstveno ime Bombina variegata) spada v družino žab urhov Bombinatoridae. Vpisan je na seznam ogroženih živalskih vrst v Sloveniji.
Gulbukig klockgroda (Bombina variegata[3]) är en art i familjen Bombinatoridae som tillhör ordningen stjärtlösa groddjur.
Paddliknande groda med ryggen tätt besatt med vårtor. Framtårna är skilda och bakre tårna förenade genom simhud. Ryggen har en gråbrun eller olivgrön färg och undersidan är blåsvart med klargula till orange fläckar. Längden går upp till 55 mm. Ögonen är uppåtriktade och pupillen triangelformad[4]. Den är mycket lik klockgrodan, men skiljs från denna genom bukfärgen.
Den gulbukiga klockgrodans utbredningsområde sträcker sig från mellersta Frankrike, södra Tyskland, Schweiz, italienska fastlandet (med isolerade förekomster på Sicilien), Karpaterna och Balkan. Den har introducerats i Storbritannien, men populationens öde är okänt.[5].
Den gulbukiga klockgrodan är en sällskaplig art som vistas i eller nära vatten som sjöar, dammar, bäckar, floder, flodängar, träskmarker, tillfälliga vattensamlingar, skog (barrskog, lövskog såväl som blandskog). Den går högre upp än klockgrodan, och återfinns oftast på höjder mellan 100 och 2 100 m.[5] Lätet är melodiskt, men svagare än klockgrodans. Den är främst dagaktiv, men kan vara i rörelse även nattetid.[4] Arten har insekter, daggmaskar och blötdjur som föda.[6]
Den är inaktiv under vintern, från november till februari[4].
Arten kan vandra en längre sträcka från vintergömstället till platsen där den fortplanta sig.[6] Den gulbukiga klockgrodan leker i april till augusti. Amplexus (hanens omklamrande av honan i samband med leken) sker strax framför bakbenen.[4]
Äggen lägges lösa eller i mindre klumpar på vattenväxter[4]. Cirka efter åtta dagar kläcks äggen. Den första metamorfosen sker efter cirka en månad och de full utvecklade grodorna är ungefär 15 mm långa. Ibland övervintrar ofullständig utvecklade individer. Ungarna blir könsmogna under tredje levnadsåret och vissa exemplar kan leva 26 år.[6]
Gulbukig klockgroda (Bombina variegata) är en art i familjen Bombinatoridae som tillhör ordningen stjärtlösa groddjur.
Жовточерева джерелянка характеризується доволі високою екологічною пластичністю у виборі біотопів, її можна знайти у різноманітних місцях пробування: у хвойних, листяних та мішаних лісах, на полонинах, у чагарниках, на луках та в полях. Тут вона трапляється не тільки в стоячих чи слабопроточних водоймах (озера, стави, калюжі, канали, водосховища), але іноді й у водоймах з відносно швидкою течією (по берегах струмків та річок).
В Україні жовточерева джерелянка зустрічається у гірських та передгірських районах Карпат, де піднімається до висоти близько 2000 м. У Закарпатській області трапляється майже повсюдно, за винятком крайніх південно-західних рівнинних ділянок. У Львівській області перебування виду пов'язано з гірсько-передгірською південно-західною частиною й доходить на північ до Перемишлянського та Старосамбірського районів.
Існують відомості, що в Карпатах жовточереві джерелянки менш вимогливі до рівня забрудненості води, ніж B.(B.) bombina, і можуть заселяти водойми з доволі високим насиченням органікою, високою солоністю та навіть жити у мінеральних джерелах.
В Івано-Франківській області трапляється майже на всій території (хоча не знайдена у її північній частині). Поширення у Чернівецькій області прив'язано до її західних районів, на схід доходить до м. Чернівці. Відомо декілька знахідок жовточеревої джерелянки у західній частині Тернопільської області (Бучацький та Гусятинський р-ни), що потребує перевірки.
Щільність B.(B.) variegata на більшій частині її ареалу в межах України доволі висока (часто перевищує 1 особину на 0,02-20 м²). За матеріалами маршрутних обліків їхня чисельність коливалася від 10 до 50 особин на 100 м берегової лінії. Найбільша чисельність відзначена у невеликих водоймах у передгір'ях та низькогір'ях на висотах від 350–600 до 900 м.
Досліджень вікової структури окремих популяцій цього виду в Україні брак, або вони вкрай обмежені. Мічення жовточеревих джерелянок у західних ділянках їхнього ареалу (Австрія) показало, що в 1985 р. 1090 особин представляли близько 91% чисельності всієї популяції. Повторні відлови цих амфібій у 1991 р. дозволили встановити, що вік мічених тварин становить 9-10 років і на них припадало понад двох третин (78,1%) чисельності всієї популяції. Вік самців жовточеревої джерелянки в Італії становить 8,0 ± 2,4 років, а самиць 8,3 ± 1,8. При цьому найстарші самці досягають 16-річного, а самиці — 14-річного віку.
Амфібії невеликих розмірів, довжина тулуба 27-50 мм, забарвлення спинного боку тіла зазвичай оливково-зеленкуватих тонів з невиразними дрібними темними плямами. Черевна частина яскравого забарвлення, представлена жовтим чи помаранчевим тлом із великими темними плямами, площа жовто-помаранчевого тла звичайно перевищує площу темних плям. Жовто-помаранчеве тло черевної частини переходить на нижню частину задніх кінцівок.
На спинному боці добре розвинені горбки, що закінчуються гострими шипиками. У самців резонаторів брак. В них же в шлюбний сезон на перших трьох пальцях передніх кінцівок та на нижньому боці передрамен розвиваються шлюбні мозолі.
Іноді трапляються джерелянки з зеленим забарвленням спини (зелені морфи), їх вивчення показало, що розвиток цієї ознаки залежить від особливостей генотипу й має адаптивний характер. Вид поширений у Європі, де притаманний гірським районам, однак відсутній на Іберійському півострові та на півночі Італії (долина р. По), на сході його поширення обмежене Українськими Карпатами; межа ареалу на півночі не доходить до прибережних районів Франції, Німеччини, Данії (в Англії інтродукований). Живе на більшій частині Апеннінського та Балканського півостровів.
Зараз розрізняють 2-4 підвиди кумки жовточеревої. При цьому не виключено, що апеннінський підвид B. (B.) variegata pachypus та балканський підвид B. (B.) variegata scabra, є окремими видами.
Українські популяції відносяться до номінативного підвиду.
Дані досліджень морфологічної мінливості українських популяцій обмежені порівнянням прикарпатських та закарпатських популяцій. Результати показали, що статистично достовірні відміни властиві 4 з 5 узятих для порівняння показників: L. 43,04 і 35,29; F. 15,95 і 13,29; T. 15,85 і 13,52; F./T. 1,005 і 0,91 (для Закарпаття та Прикарпаття відповідно; розміри в мм). Ряд достовірних відмін відзначений також для B. (B.) variegata, що живуть у Закарпатті на великих висотах при порівнянні з кумками з низько- та середньогір'їв.
Середні розміри самців жовточеревої джерелянки в інших ділянках ареалу (Італія) становлять 46,1 ± 3,0 мм, самиць — 46,8 ± 3,5 мм. Порівняння зовнішньої морфології самців та самиць на Балканах виявило, що самиці істотно більші від самців. Разом з тим відзначається сильний вплив географічної мінливості. Оцінюючи міжвидові відмінності B.(B.) variegata і B.(B.) scabra у порівнянні з B.(B.) bombina, автори зазначають, що коли усунути вплив географічної (міжпопуляційної) мінливості то тоді виразно виявляються міжстатеві відмінності між представниками трьох таксонів за довжиною стегна.
Крім того, у B.(B.) scabra виявляється статевий диморфізм за довжиною плеча, а в червоночеревих джерелянок за довжиною голови. Ознаки, характерні для цього виду (особливості візерунка та горбчастості жовточеревих джерелянок), можуть з різною частотою проявлятися в популяціях іншого виду — червоночеревої джерелянки (Московська обл. Росії); у жовточеревих джерелянок, що живуть навіть у притаманних ним високогірних біотопах, частка ознак, властивих іншому видові, може сягати 8,3-21,5%.
Диплоїдний набір містить 24 двоплечі хромосоми (2n = 24,NF = 48).На коротких плечах 7-ї пари хромосом у B.(B.) variegata pachypus з Італії виявлені ядерцеві організатори (як вже зазначалося, не виключено, що це окремий вид) (Odierna et al., 2000).
Кількість ДНК кумки жовточеревої на Балканах на 5,5% нижча, ніж у B.(B.) bombina, а рівні мінливості цього показника в обох видів не перекриваються. Цікаво, що балканський підвид B.(B.) variegata scabra ближчий до B.(B.) bombina, ніж до номінативного підвиду B.(B.) variegata. Понадто, в представників обох підвидів B.(B.) variegata рівні мінливості ДНК також не перекриваються, на відміну від B.(B.) variegata scabra і B.(B.) bombina.
На Закарпатті зона схрещування між обома видами джерелянок (шириною 1-10 км) розташована на висоті 120–200 м. Однак при віддаленні від цієї зони ступінь наявності в жовточеревої джерелянки «нетипових» для неї генів B.(B.) bombina різна. Так, у декількох вибірках жовточеревої джерелянки, що живе на висотах 500–600 м, 35-40% особин мають декілька алелів червоночеревої джерелянки, однак така частка алелів цього виду спадала до 2% у вибірках B.(B.) variegata, узятих на висоті 250 м.
Зона гібридизації завжди наявна в місцях пробування двох видів при переході від низини до гір, утворювані гібриди зазвичай плодючі. У природних та одержаних в лабораторних умовах гібридів першого покоління функціонують обидва батьківські алелі.
Висота розташування зони гібридизації коливається від 110 м на території колишньої Югославії до 300–400 м у Нижній Австрії. Разом з тим у східній Словаччині червоночерева джерелянка може траплятися на великих висотах (плато), а B.(B.) variegata — на менших (річкова долина). У цьому ж районі виявлені гібриди. Така ситуація пояснюється місцевими кліматичними особливостями та більш комфортними умовами на відносно великих висотах.
У самців першого покоління, одержаних штучним схрещуванням, сперматогенез був порушений на рівні утворення сперматозоїдів, хоча оогенез у самиць проходив нормально. В гібридів другого покоління (схрещували гібридних самиць першого покоління з батьківськими особинами) порушення відбувалися як при оогенезі, так і при сперматогенезі.
Початок сезонної активності на Закарпатті зазвичай припадає на першу половину березня, а в Прикарпатті — на кінець березня — початок квітня. Оселяється у водоймах з повільною течією, у стоячих водоймах де перебуває майже весь час. Майже відразу ж після пробудження (приблизно за 5-10 діб) при прогріванні води до 12-14°С тварини приступають до парування та відкладання ікри. Період відкладання ікри розтягнутий і може тривати до серпня, при цьому в одній і той самій водоймі можуть бути не тільки особини в амплексусі, але також і пуголовки з різним ступенем розвитку кінцівок, або такі, що проходять метаморфоз.
Звичайно самиця відкладає близько 100–200 ікринок у вигляді однієї або кількох порційних кладок (по 10-30), часто прикріплюючи їх до різних підводних предметів: рослин, гілля, каменів. Тривалість ембріогенезу значною мірою залежить від температури води й становить приблизно 5-12 діб. При лабораторному дослідженні фенотипової пластичності (личинок вирощували за різних температур) було встановлено, що цей фактор не справляє істотного впливу на мінливість розмірів при метаморфозі. Розміри щойно вилуплених пуголовків 5-7 мм (довжина тіла з хвостом).
Будова ротового апарату личинок відрізняється від такого в червоночеревої джерелянки. Початок метаморфозу відзначений при довжині тіла личинок 45-50 мм. Метаморфоз завершується, в середньому, за два або більше місяців. Розміри тіла цьоголітків відразу після метаморфозу становлять 16-20 мм. Значна частина пуголовків зимує у воді, метаморфоз відбувається на 2 рік.
Статевозрілість настає на другому або третьому році життя. Методом мічення жовточеревих джерелянок в Австрії встановлено, що репродуктивна активність цього виду триває приблизно 2-14 років, а найбільший вік становить близько 15 років.
Жовточереві джерелянки менш прив'язані до водойм, ніж B. (B.) bombina. Однак для них також є характерним збільшення міграційної активності в періоди дощів та при вологій погоді. При порівнянні добової активності жовточеревої та червоночеревої джерелянок особливих відмінностей не помічено, вони приблизно схожі.
Початок зимівлі часто залежить від погодних умов та висоти пробування, він найчастіше припадає на кінець вересня — початок листопада. Зазвичай зимівля проходить на суші в порожнинах під, лежачими деревами, під камінням, в льохах, підвалах, хоча активних жовточеревих джерелянок інколи помічали у воді термальних джерел і взимку. На зимівлях відзначена разом з іншими видами не лише амфібій (тритони, ропухи, жаби), але й рептилій — живородні ящірки, звичайні вужі.
На здобич полює у воді чи біля водойм. Склад їжі жовточеревих джерелянок відрізняється від B.(B.) bombina дещо більшою кількістю безхребетних, що живуть на суші (іноді до 81%). Так, у їхньому раціоні відмічені Formicidae (до 15-36,8%), наземні форми Diptera (13,2-16,8%); істотна частка різних видів молюсків, жуків (іноді до 78,3%) тощо. Відомі випадки канібалізму.
Серед природних ворогів B.(B.) variegata, так само як і червоночеревої джерелянки, вказано чимало біляводних хребетних: їхніх личинок поїдають тритони (Triturus cristatus), дорослих тварин — вужі (водяний та звичайний), деякі види птахів (лелека, чапля та ін.).
Жовточеревим джерелянкам також притаманна своєрідна захисна поведінка у формі демонстрації апосематичного забарвлення — яскраво забарвленого черева та нижнього боку кінцівок.
Вид занесено до Додатку II «Конвенції з охорони дикої флори і фауни та природного середовища існування в Європі» (категорія «види, що підлягають особливій охороні») та до «Червоної книги хребетних Міжнародного союзу охорони природи (МСОП)», а також включено до третього видання «Червоної книги України» (категорія «вразливі види»).
Cóc tía bụng vàng (danh pháp hai phần: Bombina variegata) là một loài cóc thuộc chi Cóc tía.
Phương tiện liên quan tới Bombina_variegata tại Wikimedia Commons
Cóc tía bụng vàng (danh pháp hai phần: Bombina variegata) là một loài cóc thuộc chi Cóc tía.
Bombina variegata (Linnaeus, 1758)
Ареал
Bombina variegata
Желтобрюхая жерлянка[1][2] (лат. Bombina variegata) — вид бесхвостых земноводных из семейства жерлянок.
Взрослые жерлянки редко достигают 35—55 мм в длину. Окрас: верх буроватый, серо-коричневый до тёмно-оливкового, с тёмными или грязно-зелёными пятнами. Брюхо жёлтое с чёрно-серыми неровными пятнами и разводами. Узор пятен индивидуален для каждой лягушки. Концы пальцев как сверху, так и снизу светлые (жёлтые).
Период размножения — конец весны и начало лета.
Икринки сверху коричневые, снизу — светло-коричневые, около 1,5—2 мм в диаметре.
Головастики грязно-серого цвета, на солнце переливаются.
Желтобрюхая жерлянка включена в категорию LC Красного списка МСОП. Она обитает в большей части Южной и Центральной Европы, в ручьях, болотах, реках, озёрах, водохранилищах, на высоте 100—2100 м над уровнем моря. Была занесена в Великобританию, однако достоверно не известно, сохранились ли там популяции жерлянки.
Желтобрюхая жерлянка (лат. Bombina variegata) — вид бесхвостых земноводных из семейства жерлянок.
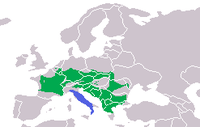
多彩铃蟾(学名:Bombina variegata)是两栖纲无尾目铃蟾科铃蟾属的一种,分布于欧洲地区。成蛙4~5厘米,背部为灰褐色,腹部黄色或橙色,有深色斑点。遇到危险时会将腹部朝上,露出警示色,并分泌毒液。
 保全状況評価[1] LEAST CONCERN
保全状況評価[1] LEAST CONCERN 分類 界 : 動物界 Animalia 門 : 脊索動物門 Chordata 亜門 : 脊椎動物亜門 Vertebrata 綱 : 両生綱 Amphibia 目 : 無尾目 Anura 科 : スズガエル科 Bombinatoridae 属 : スズガエル属 Bombina 種 : キバラスズガエル B. variegata 学名 Bombina variegata
分類 界 : 動物界 Animalia 門 : 脊索動物門 Chordata 亜門 : 脊椎動物亜門 Vertebrata 綱 : 両生綱 Amphibia 目 : 無尾目 Anura 科 : スズガエル科 Bombinatoridae 属 : スズガエル属 Bombina 種 : キバラスズガエル B. variegata 学名 Bombina variegata
キバラスズガエル(黄腹鈴蛙、Bombina variegata)はスズガエル科に分類されるカエルの一種。
アルバニア、イタリア、ウクライナ西部、オーストリア、オランダ、ギリシャ、クロアチア、スイス、スウェーデン、スロバキア、セルビア、チェコ、ドイツ南部、ハンガリー、ブルガリア、ベルギー、ボスニア・ヘルツェゴビナ、ポーランド南部、マケドニア共和国、モンテネグロ、モルドバ南部、ルクセンブルク、ルーマニア
体長4-5cm。体は扁平で背面は緑がかった褐色や灰色に小型の黒い斑紋、腹面は黄色やオレンジで小型の黒い不規則な斑紋が入る。腹面には白い斑点がないか少ない。皮膚にはイボがあるがスズガエル属の別種ヨーロッパスズガエルに比べると小さく目立たない。
ヨーロッパスズガエルと分布が重なる場所では種間雑種を作ることもある。
草原や森林にある河川や池の周辺生息する。水質汚濁に強いのか、あまり水が綺麗でない場所にも生息する。皮膚から毒液を分泌し、外敵に襲われると四肢と体を反ったりひっくり返り腹部の派手な警戒色を見せる対捕食者姿勢をとる。秋になると穴を掘り、その中で冬眠を行う。
繁殖形態は卵生で、冬眠から目覚めた後に岩の下や水草等に不規則な卵塊を産む。
ペットとして飼育されることもあり、日本にも輸入される。流通量は少ない。
本種に限ったことではないが皮膚に毒を持つので基本的には素手で触れたりせず(カエルとしてもストレスになったり、人間の体温は高温過ぎるため)、触った時には必ず手を洗うようにする。
|date= (help)CS1 maint: Uses authors parameter
봄비나 바리에가타는 개구리목 무당개구리과의 양서류로, 한국의 무당개구리와 같은 속의 개구리이다. 영어권에서는 노란배두꺼비(Yellow-bellid toad)라고 한다.
몸길이는 4-5cm이다. 등 색깔은 회갈색이고, 밝은색 반점이 있다. 동공은 하트 모양이고, 고막은 눈에띄지 않는다. 배의 색깔은 회청색 또는 검은색이고 밝은 노란색 반점이 있다.
초원, 숲이 있는 하천, 연못의 주변에 서식한다. 늦은 봄과 이른 여름에 짝짓기를 한다.
식성은 육식성으로 곤충이나 갑각류, 지렁이 등을 먹는다.